题目内容
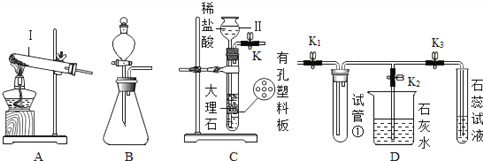
【题目】如图所示为实验室中常见的气体制备、干燥、收集和性质实验的部分仪器(组装实验装置时,可重复选择仪器)。试根据题目要求,回答下列问题:
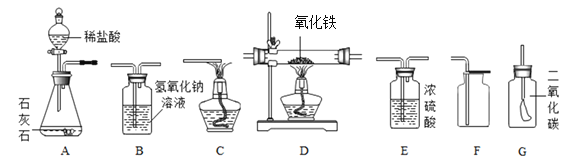
(1)欲在实验室中制备并收集干燥的二氧化碳气体。
①所选仪器的连接顺序为_________________(填写仪器序号字母)。
②仪器A中,发生反应的化学方程式为_____________________。
③若向G装置中倒入适量澄清石灰水,迅速用预先绑有小气球的橡皮塞塞紧,振荡,观察到的气球出现的现象是_______________________。
(2)欲用混有少量二氧化碳的一氧化碳气体还原氧化铁,所选仪器的连接顺序为:混合气体→D→B→C。进行实验时,D装置玻璃管中的现象是___________。
【答案】 A-E-F CaCO3+2HCl=CaCl2+CO2 +H2O 气球鼓起 红棕色固体变黑
【解析】(1)①实验室通常用稀盐酸与大理石反应制取二氧化碳,反应物的状态是固态和液态,反应条件是常温,应选固液不加热型的发生装置;二氧化碳的密度比空气大,能溶于水,不能用排水法收集;因为要收集到干燥的二氧化碳,所以应在收集装置前面加一个干燥装置,浓硫酸具有吸水性,可用来干燥二氧化碳,所以仪器的连接顺序为:A→E→F;②A中反应物是碳酸钙和盐酸,生成物是氯化钙、水、二氧化碳,,反应的方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑;③二氧化碳能与氢氧化钙反应生成碳酸钙和水,二氧化碳被消耗,则瓶内的压强小于大气压,在大气压的作用下,小气球会鼓起;(2)①一氧化碳是可燃性气体,与空气混合后加热有爆炸的危险,所以为排净玻璃管中的空气,防止加热时发生爆炸,进行实验时,要先向D装置的玻璃管中通一会儿CO,然后加热,一氧化碳和氧化铁在高温的条件下反应生成铁和二氧化碳,故D装置玻璃管中的现象是:红棕色固体变黑。

【题目】同学们通过学习金属后,对铜的化学性质进行了进一步的研究。
项目一. 同学们将光亮铜片放在酒精灯火焰上灼烧,发现表面变黑,他们对黑色物质来源产生了兴趣,铜片表面黑色物质是什么呢?
【查阅资料】
(1)酒精不充分燃烧产生炭黑(即黑烟);
(2)氧气的化学性质比较活泼,加热条件下能与金属铜反应生成黑色的氧化铜。
(3)氧化铜能与硫酸反应生成硫酸铜和水;炭黑难溶于水,且与硫酸不发生反应。
【猜想与假设】
猜想1:黑色固体是炭黑。
猜想2:黑色固体是空气中的氧气与铜反应生成的氧化铜。
猜想3:黑色固体既有炭黑又有氧化铜。
【进行实验】
实验步骤和方法 | 实验现象 | 实验结论 |
实验一:取一小段光亮铜片,放入试管内,然后用试管夹夹持试管,放在酒精灯的外焰部位加热。 | 铜片变黑 | (1)猜想1不正确。 (2)黑色固体可能与空气中的 ______ 有关。 |
实验二:取一试管,将一小段光亮铜片放入试管中,塞上胶塞,并用注射器抽出试管内的空气,封好胶塞,并加热,观察现象。趁热取下胶塞,观察现象。 | ________ | 猜想2正确 |
实验三:将在酒精灯火焰上灼烧后的附着黑色固体的铜片,投入到盛有稀硫酸的试管中。 | ________ | 猜想3不正确 |
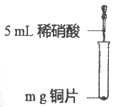
项目二. 同学们通过学习知道铜与盐酸、稀硫酸不能发生反应,但却发现化学老师用铜与硝酸制备出气体去做物理实验。同学们在实验室对铜与稀硝酸的反应进行了探究。
实验I | |
实验装置 | 实验现象 |
| 铜片逐渐消失, 有无色气泡产生,试管中上部有红棕色气体出现; 溶液由无色变为蓝色 |
【探究】实验I中产生的无色气体是什么?
【查阅资料】
(1)硝酸(HNO3)与Cu反应生成硝酸铜和含氮元素的化合物;硝酸铜溶液呈蓝色;
(2)氨气(NH3)可以使酚酞溶液变红
(3)含氮元素的某些气态物质的物理性质
NH3 | NO | NO2 | |
颜色 | 无色 | 无色 | 红棕色 |
气味 | 刺激性 | 刺激性 | |
溶解性 | 极易溶于水 | 难溶于水 | 可溶于水或硝酸 |
【猜想与假设】无色气体可能是:①NH3 ②NO
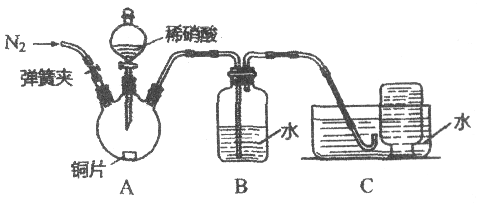
【进行实验】同学们利用下图装置对产生的无色气体进行检验。
实验操作 | 实验现象 |
1. 打开弹簧夹,通入N2,一段时间后,关闭弹簧夹 | B、C中导管口有无色气泡冒出 |
2. 将C中导管伸入集气瓶中,打开分液漏斗的活塞,滴入一定量稀硝酸,关闭活塞 | A中有无色气泡产生 B中导管口有无色气泡冒出 C中集气瓶内收集到无色气体 |
3. 从水槽中取出集气瓶,敞口置于空气中 | 无色气体变为红棕色 |
4. 取少量B中液体于试管中,滴加无色酚酞溶液 | 试管中溶液颜色无明显变化 |
【解释与结论】
(1)操作1中,通入N2的目的是__________。
(2)同学们认为猜想①不正确,理由是__________。
(3)无色气体具有的化学性质是__________。