题目内容
用来测定空气成分的方法很多,如图1所示的是用红磷在空气中燃烧的测定方法.实验过程是:
第一步:将集气瓶容积划分为五等份,并做好记.
第二步:点燃燃烧匙内的红磷,伸入集气瓶中并把塞子塞紧.
第三步:待红磷熄灭并冷却后,打开弹簧夹,发现水被吸入集气瓶
中,进入集气瓶中水的体积约为集气瓶总容积的
.
请回答下列问题:

(1)上述实验现象
文字表达式为
(2)该实验中的红磷能用硫取代吗?
(3)实验完毕,若进入集气瓶中水的体积不到总容积的
,你认为导致这一结果的原因能是
(4)某同学对实验进行反思后,提出了改进方法(如图2所示 ),你认为改进后的优点是:
第一步:将集气瓶容积划分为五等份,并做好记.
第二步:点燃燃烧匙内的红磷,伸入集气瓶中并把塞子塞紧.
第三步:待红磷熄灭并冷却后,打开弹簧夹,发现水被吸入集气瓶
中,进入集气瓶中水的体积约为集气瓶总容积的
| 1 |
| 5 |
请回答下列问题:

(1)上述实验现象
红磷燃烧产生大量白烟,待红磷熄灭并冷却后打开弹簧夹,水被吸入集气瓶
中,进入集气瓶中水的体积约为集气瓶总容积的
中,进入集气瓶中水的体积约为集气瓶总容积的
| 1 |
| 5 |
红磷燃烧产生大量白烟,待红磷熄灭并冷却后打开弹簧夹,水被吸入集气瓶
中,进入集气瓶中水的体积约为集气瓶总容积的
,中,进入集气瓶中水的体积约为集气瓶总容积的
| 1 |
| 5 |
文字表达式为
磷+氧气
五氧化二磷
| 点燃 |
磷+氧气
五氧化二磷
,氮气的化学性质| 点燃 |
不活泼
不活泼
(“活泼”或“不活泼”).(2)该实验中的红磷能用硫取代吗?
不能
不能
(“能”或“不能”),硫燃烧的文字表达式为硫+氧气
二氧化硫
| 点燃 |
硫+氧气
二氧化硫
.| 点燃 |
(3)实验完毕,若进入集气瓶中水的体积不到总容积的
| 1 |
| 5 |
装置漏气
装置漏气
、红磷的量不足
红磷的量不足
、未等到装置冷却到室温就打开了止水夹
未等到装置冷却到室温就打开了止水夹
.(至少写三条)(4)某同学对实验进行反思后,提出了改进方法(如图2所示 ),你认为改进后的优点是:
误差少或无污染
误差少或无污染
.分析:(1)根据红磷的燃烧、瓶内压强的变化,水会进入集气瓶回答实验的现象;根据反应写出反应的文字表达式;剩余的气体主要氮气据此分析氮气的性质.
(2)根据硫燃烧的产物是气体分析不能红磷能用硫取代的原因,写出反应的文字表达式.
(3)根据实验的注意事项分析入集气瓶中水的体积不到总容积的
的原因.
(4)根据装置的不同点对比分析优点.
(2)根据硫燃烧的产物是气体分析不能红磷能用硫取代的原因,写出反应的文字表达式.
(3)根据实验的注意事项分析入集气瓶中水的体积不到总容积的
| 1 |
| 5 |
(4)根据装置的不同点对比分析优点.
解答:解:(1)上述实验现象是:红磷燃烧产生大量白烟,待红磷熄灭并冷却后打开弹簧夹,水被吸入集气瓶中,进入集气瓶中水的体积约为集气瓶总容积的
;瓶内剩余的气体主要是氮气,说明了氮气的性质不活泼.
(2)由于硫燃烧的生成了二氧化硫气体,装置内的压强不变,不能红磷能用硫取代.反应的文字表达式是:硫+氧气
二氧化硫.
(3)实验完毕,若进入集气瓶中水的体积不到总容积的
,导致这一结果的原因可能是:装置漏气、红磷的量不足、未等到装置冷却到室温就打开了止水夹等.
(4)通过凸透镜聚光引燃红磷,不需要打开瓶塞,空气出不来也进不去,测量比较准确.用酒精灯引燃红磷,红磷燃烧生成了五氧化二磷进入空气会污染空气,由于磷燃烧放出大量的热,打开瓶塞时容易使空气受热而逸出.所以实验的优点是:误差少或无污染.
故答为:(1)红磷燃烧产生大量白烟,待红磷熄灭并冷却后打开弹簧夹,发现水被吸入集气瓶中,进入集气瓶中水的体积约为集气瓶总容积的
;不活泼.
(2)不能;硫+氧气
二氧化硫.
(3)装置漏气、红磷的量不足、未等到装置冷却到室温就打开了止水夹等.
(4)误差少或无污染
| 1 |
| 5 |
(2)由于硫燃烧的生成了二氧化硫气体,装置内的压强不变,不能红磷能用硫取代.反应的文字表达式是:硫+氧气
| 点燃 |
(3)实验完毕,若进入集气瓶中水的体积不到总容积的
| 1 |
| 5 |
(4)通过凸透镜聚光引燃红磷,不需要打开瓶塞,空气出不来也进不去,测量比较准确.用酒精灯引燃红磷,红磷燃烧生成了五氧化二磷进入空气会污染空气,由于磷燃烧放出大量的热,打开瓶塞时容易使空气受热而逸出.所以实验的优点是:误差少或无污染.
故答为:(1)红磷燃烧产生大量白烟,待红磷熄灭并冷却后打开弹簧夹,发现水被吸入集气瓶中,进入集气瓶中水的体积约为集气瓶总容积的
| 1 |
| 5 |
(2)不能;硫+氧气
| 点燃 |
(3)装置漏气、红磷的量不足、未等到装置冷却到室温就打开了止水夹等.
(4)误差少或无污染
点评:空气是人类宝贵的自然资源,在中考中占有重要的地位,特别是空气中氧气含量的测定,要注意测定原理、实验关键、现象和结论等内容的考查

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案
相关题目
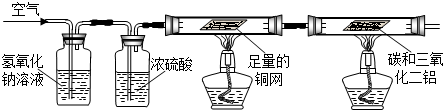
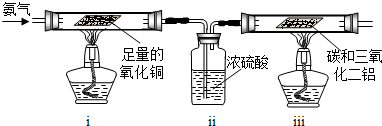
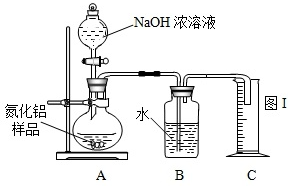
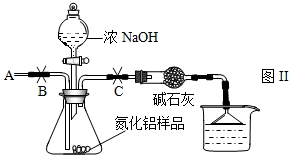
 NH3↑+CO2↑+H2O;②2NH3+H2SO4=(NH4)2SO4;③2NH3+3CuO
NH3↑+CO2↑+H2O;②2NH3+H2SO4=(NH4)2SO4;③2NH3+3CuO
