题目内容
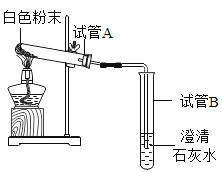
【题目】某化学兴趣小组获得一包白色粉末状固体,现拟探究这包白色固体的成分,取少量固体于试管中,加水溶解,逐滴加入盐酸溶液,产生了能使澄清石灰水变浑浊的气体。于是同学们对这包白色固体成分进行了如下猜想:
(提出猜想) 猜想一、碳酸钠 猜想二、碳酸氢钠 猜想三、碳酸钠和碳酸氢钠
(查阅资料) 1.碳酸钠、碳酸氢钠溶液均呈碱性;2.碳酸钠受热不分解。
(实验探究1) 小妍、小超分别对有关猜想设计方案并进行试验:
实验操作 | 实验现象 | 实验结论 | |
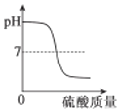
小妍 | 将白色粉末溶于水后用pH试纸测定其酸碱度 | pH____7(填“>”、“<”或“=”) | 溶液呈碱性,猜想一成立 |
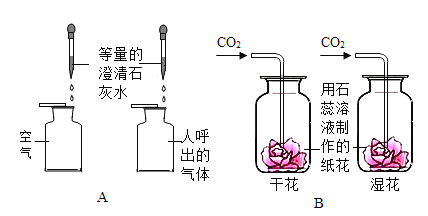
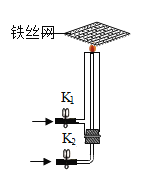
小超 | 用题图装置进行试验 | 试管A中有水珠产生,试管B中澄清石灰水变浑浊 | 猜想二成立,试管B中反应的化学方程式为: _____________________________ |
(实验质疑1)⑴小明认为小妍的实验结论不正确,理由是___________________(用文字叙述)。
⑵小芳认为小超的实验不能得出猜想二成立,理由是_______________________(用文字叙述)。
⑶该实验小组同学在向盛有白色固体的试管中加盐酸,产生了使澄清石灰水变浑浊的气体,请用化学方程式表示产生该气体的原因____________________________(写一个即可)。
(注意:若答对一下小题奖励4分,但化学试卷总分不超过60分)
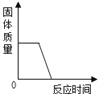
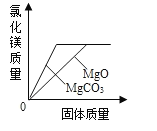
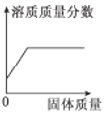
(实验探究2)为进一步确定白色粉末的化学成分,小睿称取10g白色粉末进行试验,通过计算并分析实验数据确定猜想三成立。请你帮助小睿同学设计试验方案来测定一个实验数据m,请问此实验数据m是______________________,并计算该数据m的取值范围__________________。
【答案】> ![]() 碳酸氢钠溶液也呈碱性(合理即可) 加热碳酸钠和碳酸氢钠混合物也有相同的实验现象
碳酸氢钠溶液也呈碱性(合理即可) 加热碳酸钠和碳酸氢钠混合物也有相同的实验现象 ![]() 与盐酸反应产生的二氧化碳质量
与盐酸反应产生的二氧化碳质量 ![]() <m<
<m<![]()
【解析】
[实验探究1]溶液显碱性时,其pH>7;故填:>;
二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水;故填:Ca(OH)2 +CO2 =CaCO3↓+H2O;
[实验质疑1](1)碳酸钠溶液和碳酸氢钠溶液均显碱性,所以妍的实验结论不正确,故填:碳酸氢钠溶液也呈碱性(合理即可);
(2)加热碳酸钠和碳酸氢钠混合物时,其中的碳酸氢钠会分解产生水、二氧化碳和碳酸钠,与加热碳酸氢钠时的现象相同,所以小超的实验不能得出猜想二成立,故填:加热碳酸钠和碳酸氢钠混合物也有相同的实验现象;
(3)碳酸钠和碳酸氢钠均能与盐酸反应生成氯化钠、水和二氧化碳;故填:Na2CO3+2HCl=2NaCl+H2O+CO2↑或 NaHCO3+HCl=NaCl+H2O+CO2↑;
[实验探究2]为进一步确定白色粉末的化学成分,小睿称取10g白色粉末进行试验,通过计算并分析实验数据确定猜想三成立。请你帮助小睿同学设计试验方案来测定一个实验数据m--与盐酸反应产生的二氧化碳质量;
假设该白色固体是碳酸钠,设生成二氧化碳的质量为x,则:
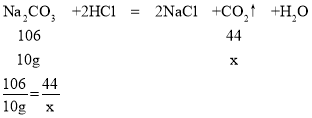
x=![]() g
g
假设该白色固体是碳酸氢钠,设生成二氧化碳的质量为y,则:
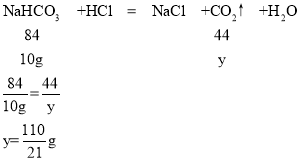
所以数据m的取值范围为![]() <m<
<m<![]() ;
;
故填:与盐酸反应产生的二氧化碳质量;![]() <m<
<m<![]() 。
。