题目内容
【题目】向某铁粉样品中,加入溶质质量分数为16%的硫酸铜溶液100 g,恰好完全反应,样品中杂质不溶于水也不与硫酸铜反应。请结合如图提供的数据计算。
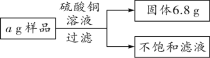
(1)求a的数值。
(2)向不饱和滤液中加入100.8 g水,求所得溶液中溶质的质量分数。(保留一位小数)
【答案】(1)6.0(2)7.6%
【解析】
解:(1)硫酸铜的质量为100 g×16%=16 g
设样品中铁的质量为x,生成铜的质量为y,生成硫酸亚铁的质量为z
Fe+CuSO4=== FeSO4+Cu
56 160 152 64
x 16 g z y
![]() =
=![]() x=5.6 g
x=5.6 g
![]() =
=![]() y=6.4 g
y=6.4 g
![]() =
=![]() z=15.2 g
z=15.2 g
a=5.6 g+(6.8 g-6.4 g)=6.0 g
(2)溶液的质量为5.6 g+100 g-6.4 g+100.8 g=200 g
所得溶液中溶质的质量分数为![]() ×100%=7.6%
×100%=7.6%
答:(1)a的数值为6.0。(2)所得溶液中溶质的质量分数为7.6%。

练习册系列答案
相关题目