题目内容
在实验室制氧气时,若把氯酸钾和二氧化锰按4:1的质量比均匀混合,加热到不再产生氧气为止,残余固体中,氯化钾占的质量分数为( )
| A、等于80% |
| B、大于80% |
| C、小于80% |
| D、等于100% |
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:氯酸钾在二氧化锰的催化作用下分解生成氯化钾和氧气,根据氯酸钾和二氧化锰的质量比可以计算残余固体中,氯化钾占的质量分数.
解答:解:氯酸钾中氧元素的质量分数为:
×100%=39.2%,
当有4份质量的氯酸钾完全反应时,生成氧气的质量为:4×39.2%=1.6,生成氯化钾的质量为:4-1.6=2.4,
则氯化钾占的质量分数为:
×100%=70.1%,
故选:C.
| 48 |
| 122.5 |
当有4份质量的氯酸钾完全反应时,生成氧气的质量为:4×39.2%=1.6,生成氯化钾的质量为:4-1.6=2.4,
则氯化钾占的质量分数为:
| 2.4 |
| 1+5-1.6 |
故选:C.
点评:化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.

练习册系列答案
相关题目
下列食品中,蛋白质含量最高的是( )
| A、何首乌 | B、牛肉 | C、大米 | D、苹果 |
推理是化学学习中常用的思维方法.下列推理正确的是 ( )
| A、酸能使紫色石蕊溶液变红.通入CO2后的紫色石蕊溶液变红,所以CO2是酸 |
| B、在同一化合物中,同种元素可显示不同价态 |
| C、在同一化合物中,金属元素显正价,所以非金属元素一定显负价 |
| D、溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数一定减小 |
下列判断不正确的是:( )
| A、碱的溶液一定显碱性,显碱性的溶液不一定是碱的溶液 | ||
B、在A+2B=2C 的反应中,若A、B的相对分子质量分别为a、b则C 的相对分子质量为
| ||
| C、单质一定是由同种元素组成,但同种元素组成的物质不一定是单质 | ||
| D、在A+B=C+D的反应中,若A、B、C、D都是化合物,则此反应一定是复分解反应 |
在pH值为4的溶液中,下列物质能大量共存的是( )
| A、Ba(NO3)2、CuSO4、NaCl |
| B、KNO3、NaCl、K2SO4 |
| C、Na2CO3、MgSO4、K2SO4 |
| D、NaOH、CaCl2、Na2SO4 |
现有质量相同的铁、铝、镁、钠四块金属,含有的原子数目最多的是( )
| A、铁 | B、铝 | C、镁 | D、钠 |
下列变化中,属于化学变化的是( )
| A、蜡烛熔化 | B、试管破裂 |
| C、纸张燃烧 | D、酒精挥发 |
2011年3月11日,发生在日本东北部的9.0级大地震并引发海啸,致使老旧的福岛第一核电站的一号、二号、三号、四号反应堆发生爆炸,导致放射性物质外泄进入大气.有害物质之一是碘131,碘131化学性质与碘127相同.下列关于碘131原子的说法中正确的是( )
| A、原子中质子数与中子数相等 |
| B、原子中核电荷数与核外电子数可能不等 |
| C、与碘127原子的质子数不相等 |
| D、碘131具有放射性 |
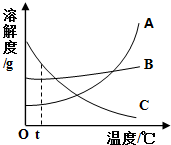 如图是A、B、C三种物质的溶解度曲线:
如图是A、B、C三种物质的溶解度曲线: