题目内容
【题目】碳酸氢钠是一种重要的盐类物质,在生活中用途广泛.小滨同学设计了实验,以探究碳酸氢钠的化学性质.
[探究实验1]碳酸氢钠溶液的酸碱性
[实验方案1]取少量该固体加入试管中,加适量水溶解,再滴入几滴酚酞溶液,振荡.
现象:溶液变成浅红色.由此得出结论________________________________________
________________________________________________________________________.
[探究实验2]能与酸反应
[实验方案2]取少量该固体加入试管中,滴加稀盐酸,现象为________________________________.
[探究实验3]碳酸氢钠的热稳定性
[实验方案3]用下图所示装置进行实验
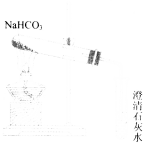
现象:充分加热后,大试管口有水珠出现,管底有白色固体残留,小试管中澄清石灰水变浑浊.
结论:碳酸氢钠受热能生成二氧化碳、水和一种白色固体.
验证:(1)请你帮小滨设计实验,证明试管中留下的白色固体是Na2CO3,而不是NaOH(所选试剂不能用酸).
步骤:________________________________________________________________________.
现象:________________________________________________________________________.
(2)碳酸氢钠受热分解的化学方程式________.
[拓展应用]试说出碳酸氢钠在日常生活中的一种用途________________________________.
【答案】[实验方案1]碳酸氢钠溶液显碱性
[实验方案2]出现气泡
(1)取少量白色固体于试管中,加适量水溶解,再滴加BaCl2[或CaCl2、Ca(OH)2、Ba(OH)2等]溶液 出现白色沉淀
(2)2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
[拓展应用]作发酵粉(或治疗胃酸过多等)
【解析】[实验方案1]根据“滴入几滴酚酞溶液,溶液变成浅红色”可知,碳酸氢钠溶液显碱性.[实验方案2]根据含有碳酸根离子或碳酸氢根离子的盐能与盐酸反应生成二氧化碳气体可知.向该固体中滴加稀盐酸,现象是出现气泡.[实验方案3]要证明试管中留下的白色固体是Na2CO3,而不是NaOH,除了采用滴加酸的方法,还可以用加入BaCl2[或CaCl2、Ca(OH)2、Ba(OH)2等溶液,观察是否出现白色沉淀的方法.根据题给信息“碳酸氢钠受热能生成二氧化碳、水和碳酸钠”即可书写化学方程式.[拓展应用]碳酸氢钠是发酵粉的主要成分,还可用于治疗胃酸过多症.

 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案