题目内容
【题目】如图是甲、乙两种固体物质的溶解度曲线。
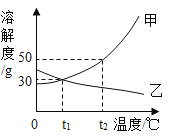
(1)t1℃时,甲、乙两种物质的溶解度___。
(2)t2℃时,将等质量的甲、乙两种物质加水溶解配制成饱和溶液,所得溶液质量的大小关系为:甲___乙(填“>”、“=”或“<”)。
(3)把一瓶接近饱和的甲物质的溶液变为饱和溶液,可行的方法是___。(答一种方法即可)
(4)甲中含少量乙,若要提取纯净的甲物质,具体的操作是___。
【答案】相同 < 增加溶质 降温结晶
【解析】
(1)通过分析溶解度曲线可知,t1℃时,甲、乙两种物质的溶解度相同。
(2)t2℃时,甲物质的溶解度大于乙物质的溶解度,所以将等质量的甲、乙两种物质加水溶解配制成饱和溶液,所得溶液质量的大小关系为:甲<乙。
(3)把一瓶接近饱和的甲物质的溶液变为饱和溶液,可行的方法是增加溶质。
(4)甲物质的溶解度受温度变化影响较大,所以甲中含少量乙,若要提取纯净的甲物质,具体的操作是降温结晶。

练习册系列答案
相关题目
【题目】下列选用的除杂试剂和实验操作都正确的是(括号内为杂质)
选项 | 物质 | 除杂选用的试剂和操作 |
A | NaCl固体(Na2CO3)固体 | 加入足量盐酸,搅拌至充分反应,蒸发结晶 |
B | KCl固体(KClO3)固体 | 加入少量的MnO2,加热 |
C | CO2(CO) | 通入足量氧气,点燃 |
D | NaNO3溶液(NaOH溶液) | 加入适量CuSO4溶液,过滤 |
A. AB. BC. CD. D