题目内容
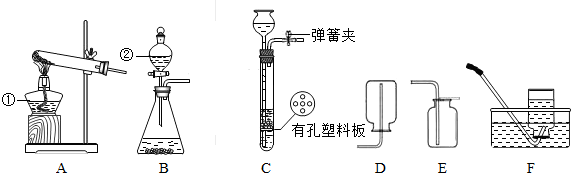
通过对化学的学习,你已掌握了实验室制取气体的有关规律,请结合图1回答问题: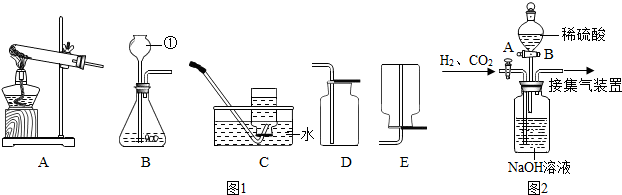
(1)图中标有①的仪器名称
(2)实验室用加热高锰酸钾的方法制取氧气,反应的化学方程式为
(3)实验室用锌和稀硫酸制取氢气,应选择的装置组合是
(4)工业常需分离H2、CO2的混合气体.某同学采用如图2所示的装置也能达到分离该混合气体的目的.操作步骤如下:
①关闭活塞B,打开活塞A,通入混合气体,可收集到
②然后,

(1)图中标有①的仪器名称
长颈漏斗
长颈漏斗
.(2)实验室用加热高锰酸钾的方法制取氧气,反应的化学方程式为
2KMnO4
K2MnO4+MnO2+O2↑
| ||
2KMnO4
K2MnO4+MnO2+O2↑
,可选择的收集装置是
| ||
C
C
或D
D
.实验时在试管口塞一小团棉花的目的是防止加热时高锰酸钾粉末进入导管
防止加热时高锰酸钾粉末进入导管
.(3)实验室用锌和稀硫酸制取氢气,应选择的装置组合是
BC或BE
BC或BE
.该发生装置也可用于实验室制取二氧化碳,反应的化学方程式为CaCO3+2HClH2O═CaCl2+CO2↑+H2O
CaCO3+2HClH2O═CaCl2+CO2↑+H2O
.(4)工业常需分离H2、CO2的混合气体.某同学采用如图2所示的装置也能达到分离该混合气体的目的.操作步骤如下:
①关闭活塞B,打开活塞A,通入混合气体,可收集到
H2
H2
气体.②然后,
关闭活塞A,打开活塞B
关闭活塞A,打开活塞B
(填操作),又可收集到另一种气体.分析:(1)熟悉常见仪器,了解名称;
(2)根据用加热高锰酸钾的方法制取氧气的反应物、反应条件、生成物写出反应方程式,据氧气的密度和溶解性选择收集装置;加热高锰酸钾时试管口要放一团棉花,防止加热时高锰酸钾粉末进入并堵塞导管;
(3)根据实验室制取氢气反应物状态和反应条件选择发生装置,据氢气密度和溶水性选择收集装置,据制取二氧化碳的反应原理书写方程式;
(4)①根据氢气不与氢氧化钠溶液反应,而二氧化碳与氢氧化钠溶液反应分析;
②根据二氧化碳与氢氧化钠溶液反应生成碳酸钠,碳酸钠与稀硫酸反应生成二氧化碳分析.
(2)根据用加热高锰酸钾的方法制取氧气的反应物、反应条件、生成物写出反应方程式,据氧气的密度和溶解性选择收集装置;加热高锰酸钾时试管口要放一团棉花,防止加热时高锰酸钾粉末进入并堵塞导管;
(3)根据实验室制取氢气反应物状态和反应条件选择发生装置,据氢气密度和溶水性选择收集装置,据制取二氧化碳的反应原理书写方程式;
(4)①根据氢气不与氢氧化钠溶液反应,而二氧化碳与氢氧化钠溶液反应分析;
②根据二氧化碳与氢氧化钠溶液反应生成碳酸钠,碳酸钠与稀硫酸反应生成二氧化碳分析.
解答:解:(1)图中①是长颈漏斗;
(2)加热高锰酸钾生成锰酸钾、二氧化锰和氧气,方程式是:2KMnO4
K2MnO4+MnO2+O2↑,氧气的密度比空气 大且不易溶于水,所以可用向上排空气法或排水法收集;加热高锰酸钾时试管口要放一团棉花,防止加热时高锰酸钾粉末进入并堵塞导管;
(3)实验室用锌和稀硫酸制取氢气不需加热,故选发生装置B,氢气的密度比空气小且难溶于水,所以可用向下排空气法或排水法收集;实验室制取二氧化碳用大理石和稀盐酸反应,生成氯化钙、水和二氧化碳,方程式是:CaCO3+2HClH2O═CaCl2+CO2↑+H2O;
(4)①氢气不与氢氧化钠溶液反应,而二氧化碳与氢氧化钠溶液反应,所以关闭活塞B,打开活塞A,通入混合气体,可收集到氢气;
②二氧化碳与氢氧化钠溶液反应生成碳酸钠,碳酸钠与稀硫酸反应生成二氧化碳,所以在完成①之后,关闭活塞A,打开活塞B,这时B中的稀硫酸与步骤①中二氧化碳与氢氧化钠溶液反应生成碳酸钠反应,生成二氧化碳,所以此时可收集到二氧化碳;
故答案为:(1)长颈漏斗;
(2)2KMnO4
K2MnO4+MnO2+O2↑; C; D; 防止加热时高锰酸钾粉末进入导管;
(3)BC或BE; CaCO3+2HClH2O═CaCl2+CO2↑+H2O;
(4)①H2; ②关闭活塞A,打开活塞B.
(2)加热高锰酸钾生成锰酸钾、二氧化锰和氧气,方程式是:2KMnO4
| ||
(3)实验室用锌和稀硫酸制取氢气不需加热,故选发生装置B,氢气的密度比空气小且难溶于水,所以可用向下排空气法或排水法收集;实验室制取二氧化碳用大理石和稀盐酸反应,生成氯化钙、水和二氧化碳,方程式是:CaCO3+2HClH2O═CaCl2+CO2↑+H2O;
(4)①氢气不与氢氧化钠溶液反应,而二氧化碳与氢氧化钠溶液反应,所以关闭活塞B,打开活塞A,通入混合气体,可收集到氢气;
②二氧化碳与氢氧化钠溶液反应生成碳酸钠,碳酸钠与稀硫酸反应生成二氧化碳,所以在完成①之后,关闭活塞A,打开活塞B,这时B中的稀硫酸与步骤①中二氧化碳与氢氧化钠溶液反应生成碳酸钠反应,生成二氧化碳,所以此时可收集到二氧化碳;
故答案为:(1)长颈漏斗;
(2)2KMnO4
| ||
(3)BC或BE; CaCO3+2HClH2O═CaCl2+CO2↑+H2O;
(4)①H2; ②关闭活塞A,打开活塞B.
点评:实验发生装置的选择要根据反应物的状态和反应条件,气体收集装置的选择要根据气体的密度和溶解性,并能结合装置选取方法、气体的性质、装置特点灵活分析解答问题.

练习册系列答案
相关题目