题目内容
【题目】某混合气体含有CO、CO2、SO2三种气体。萱萱对此进行了探究。
(查阅资料)I.SO2 能使品红溶液褪色,易与高锰酸钾溶液反应而被吸收。II.CO 和CO2均不能使品红溶液褪色,也不与高锰酸钾溶液反应。Ⅲ. CO2、SO2均能与氢氧化钠溶液反应,能使澄清的石灰水变浑浊。
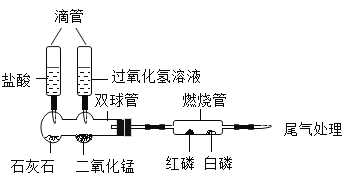
(实验探究)为验证这三种气体,萱萱在老师指导下, 设计并进行如下实验:

(事实与结论)通过实验验证了以上三种气体的存在, 请完成下列空格:
(1)装置 A中品红褪色,证明存在_____; 装置 C的作用是_____。
(2)若C没有变化,D变浑浊,证明存在_____;若结论为三种气体均存在,则装置G反应的化学方程式是_____。
(反思与评价)装置①和装置②_____(填“能”或“不能”)互换, 理由是_____。
【答案】二氧化硫 检验二氧化硫是否被高锰酸钾浓溶液完全吸收 二氧化碳 ![]() 不能 不能确定是否含有二氧化碳和二氧化硫两种气体
不能 不能确定是否含有二氧化碳和二氧化硫两种气体
【解析】
由图可知,装置①是检验并除去二氧化硫,装置②是检验并除去二氧化碳,装置G、H是验证一氧化碳的还原性和还原产物,最后处理尾气。
(1)SO2 能使品红溶液褪色,装置 A中品红变红,证明存在二氧化硫; 装置 C的作用是:检验二氧化硫是否被高锰酸钾浓溶液完全吸收。
(2)若C没有变化,说明B装置把二氧化硫完全吸收,剩余气体只有二氧化碳能使石灰水变浑浊,D变浑浊,证明存在二氧化碳;若结论为三种气体均存在,则装置G发生的反应是一氧化碳还原氧化铜,反应的化学方程式是![]() 。
。
[反思与评价]CO2、SO2均能与氢氧化钠溶液反应,能使澄清的石灰水变浑浊,装置①和装置②不能互换, 理由是不能确定是否含有二氧化碳和二氧化硫两种气体。

 名校课堂系列答案
名校课堂系列答案【题目】为了帮助同学们更好的理解空气中氧气含量测定的实验原理,老师利用传感器技术实时测定了实验装置图中图1内的压强、温度和氧气浓度,三条曲线变化如图2所示。

(1)X曲线表示的是_____(填“温度”或“氧气的浓度”)。
(2)结合X、Y两条曲线,解释图2中BC段气压变化的原因是_______。
(3)实验中测得的数据如下:
实验前 | 实验后 | ||
测量项目 | 烧杯中水的体积 | 烧杯中剩余水的体积 | 瓶中剩余气体的体积 |
体积/mL | 80.0 | 46.4 | 126.0 |
根据实验数据计算:测得的空气中氧气的体积分数为_____(列出计算式即可)。
(4)若测得的实验结果明显偏小,可能的原因是①______;②________。