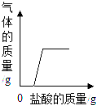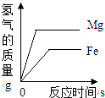题目内容
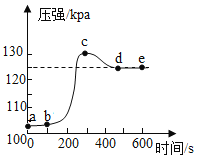
【题目】某化学兴趣小组想探究实验室中久置的NaOH的变质程度。先称取13.3 g的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入质量分数为14.6%的稀盐酸,实验测得加入稀盐酸的质量与产生CO2气体的质量关系如图所示。

(1)求称取的样品中含NaOH的质量_____。
(2)样品中NaOH的变质程度为____(已经变质的NaOH质量占未变质时NaOH的总质量的百分数)。
(3)实验过程中与NaOH反应所用盐酸的质量为_____,根据“与NaOH反应所用盐酸的质量”,对照图象,你发现的问题是____。
【答案】8g 33.3% 50g NaOH被中和后滴加稀HCl,并没有立即产生气体
【解析】
(1)设样品中含Na2CO3的质量为x

![]()
x=5.3g
故称取的样品中含NaOH的质量:13.3g-5.3g=8.0g;
(2)设变质的氢氧化钠的质量为y
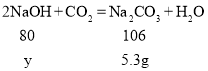
![]()
y=4.0g
故样品中NaOH的变质程度为:![]() ;
;
(3)设与氢氧化钠反应所用盐酸中溶质的质量为:
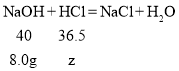
![]()
z=7.3g
所用盐酸的质量为:7.3g÷14.6%=50g
实际与氢氧化钠反应所用盐酸的质量为50g,但是由图可知,氢氧化钠被中和后,继续滴加稀盐酸,没有立即产生气体。

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
【题目】某校化学兴趣小组同学为了测定某铁合金的含铁量,做了如下实验:称取11.4g样品放入质量为50.0g的烧杯中,再往烧杯内加入足量的100.0g稀盐酸(杂质不与酸反应),并对烧杯进行了四次称量,记录的数据如下:
反应时间 | t0 | t1 | t2 | t3 |
烧杯总质量/g | 161.4 | 161.2 | 161.0 | 161.0 |
试计算:
(1) 反应产生的氢气的质量_____。
(2) 该铁合金中铁的质量分数。_____(精确到0.1%)