题目内容
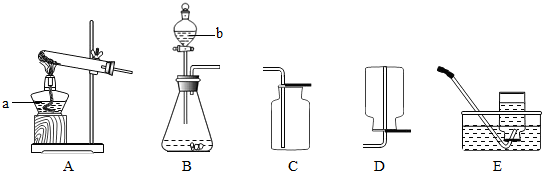
以下是实验室常见的实验装置,请回答下列问题.

(1)写出上图标示仪器的名称:①________②________;
(2)若要在实验室里制取和收集一瓶二氧化碳气体,选用的装置组合是________,(填字母标号)反应的化学方程式是________;该反应的基本类型是________.
(3)某化学兴趣小组想制取少量硝酸铜,查资料得到以下两个可行的方案:
方案一:直接用铜与稀硝酸反应,
化学方程式为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
(资料显示:NO是一种无色、难溶于水的有毒气体,密度比空气略大,常温下能与氧气迅速反应生成红棕色的有毒气体NO2.)
方案二:①灼烧铜得到氧化铜.
②氧化铜与硝酸反应,化学方程式为:CuO+2HNO3=Cu(NO3)2+2H2O
小王同学准备选用方案一,理由是步骤简单.则他选择的反应装置应该是________;(填字母标号)反应时装置中将观察到的现象有:铜片不断溶解得到蓝色溶液,________,________.
小李同学认为选用方案二比较合理,理由是________.
解:(1)熟记常用仪器的名称可知①为试管;②为酒精灯.
(2)实验室用稀盐酸与大理石反应制取二氧化碳时,反应物的状态是固态和液态,反应条件是常温,应选固-液不加热型的发生装置,二氧化碳的密度比空气大,能溶于水,只能用向上排空气法收集;碳酸钙与盐酸反应生成氯化钙、水和二氧化碳;此反应是两种化合物相互交换成份生成另外两种化合物的反应,属于复分解反应.
(3)反应物的状态是固态和液态,反应条件是常温,应选用固-液不加热型的发生装置;铜和硝酸反应生成硝酸铜、一氧化氮和水,硝酸铜溶液为蓝色,一氧化氮是气体,一氧化氮常温下能与氧气迅速反应生成红棕色的有毒气体NO2.所以该实验看到的现象是:铜片不断溶解得到蓝色溶液,有气泡冒出,瓶内出现红棕色;方案一产生的一氧化氮有毒,方案二不会产生有毒物质.
故答案为:(1)试管; 酒精灯
(2)BC; CaCO3+2HCl=CaCl2+H2O+CO2↑; 复分解反应
(3)B; 有气泡冒出; 瓶内出现红棕色; 不会产生污染环境的有害物质
分析:(1)①②均为实验室常用的仪器,熟记常用仪器的名称即可轻松作答.
(2)根据反应物的状态和反应条件确定发生装置,根据气体的密度和溶水性确定气体的收集装置;熟记常用的化学方程式;基本反应类型包括:化合反应、分解反应、置换反应、复分解反应,根据该反应的特点判断所属的基本反应类型.
(3)根据反应物的状态和反应条件确定所用的发生装置;根据生成物的特点来分析实验现象;从是否需要加热、操作是否简单、是否会造成污染、生成物是否方便使用等角度进行分析.
点评:碳酸钙与盐酸反应的生成物虽然是三种,但却属于得分解反应,二氧化碳和氢氧化钙反应生成碳酸钙和水,虽然是两种化合物反应生成两种化合物的反应,但却不属于复分解反应,因而一定要将复分解反应概念的实质弄清楚.
(2)实验室用稀盐酸与大理石反应制取二氧化碳时,反应物的状态是固态和液态,反应条件是常温,应选固-液不加热型的发生装置,二氧化碳的密度比空气大,能溶于水,只能用向上排空气法收集;碳酸钙与盐酸反应生成氯化钙、水和二氧化碳;此反应是两种化合物相互交换成份生成另外两种化合物的反应,属于复分解反应.
(3)反应物的状态是固态和液态,反应条件是常温,应选用固-液不加热型的发生装置;铜和硝酸反应生成硝酸铜、一氧化氮和水,硝酸铜溶液为蓝色,一氧化氮是气体,一氧化氮常温下能与氧气迅速反应生成红棕色的有毒气体NO2.所以该实验看到的现象是:铜片不断溶解得到蓝色溶液,有气泡冒出,瓶内出现红棕色;方案一产生的一氧化氮有毒,方案二不会产生有毒物质.
故答案为:(1)试管; 酒精灯
(2)BC; CaCO3+2HCl=CaCl2+H2O+CO2↑; 复分解反应
(3)B; 有气泡冒出; 瓶内出现红棕色; 不会产生污染环境的有害物质
分析:(1)①②均为实验室常用的仪器,熟记常用仪器的名称即可轻松作答.
(2)根据反应物的状态和反应条件确定发生装置,根据气体的密度和溶水性确定气体的收集装置;熟记常用的化学方程式;基本反应类型包括:化合反应、分解反应、置换反应、复分解反应,根据该反应的特点判断所属的基本反应类型.
(3)根据反应物的状态和反应条件确定所用的发生装置;根据生成物的特点来分析实验现象;从是否需要加热、操作是否简单、是否会造成污染、生成物是否方便使用等角度进行分析.
点评:碳酸钙与盐酸反应的生成物虽然是三种,但却属于得分解反应,二氧化碳和氢氧化钙反应生成碳酸钙和水,虽然是两种化合物反应生成两种化合物的反应,但却不属于复分解反应,因而一定要将复分解反应概念的实质弄清楚.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目

 人们的生活质量正在逐步改善,现代厨房中有许多的化学知识.
人们的生活质量正在逐步改善,现代厨房中有许多的化学知识.