题目内容
20、如图是小明配制100g溶质质量分数为12%的NaCl溶液的有关实验操作示意图.
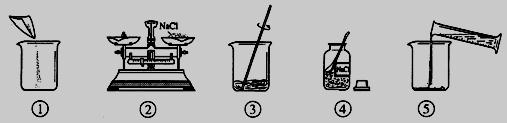
(1)配制过程中使用的四种玻璃仪器,分别是广口瓶、
(2)请你指出图中一处错误操作,并分析该操作可能造成的后果.
(3)图②、图③表示的操作步骤分别是
配制时需称量氯化钠

(1)配制过程中使用的四种玻璃仪器,分别是广口瓶、
烧杯
、玻璃棒
、量筒;(2)请你指出图中一处错误操作,并分析该操作可能造成的后果.
氯化钠和砝码位置放反,造成称量不准(或量筒中的水没有沿烧杯内壁倒入,造成液滴飞溅)
;(3)图②、图③表示的操作步骤分别是
称量、溶解
.配制时需称量氯化钠
12
g,如果氯化钠中含有少量不溶的杂质,溶质的质量分数会偏小
(填“偏大”或“偏小”);量取水最好选择③
的量筒(填序号①10mL②50mL③100mL).(水的密度为1g/cm3)分析:(1)熟记常见仪器的名称;(2)根据天平的使用注意事项来考虑;(3)根据图示可知操作步骤,根据溶质质量的计算方法来算溶质质量,根据溶质质量分数的计算公式考虑溶质质量分数的偏大偏小情况,根据量筒的选取方法推出选取量筒的量程.
解答:解:(1)熟记常见仪器的性质、用途和名称,尤其是玻璃仪器;
(2)应该左物右码,如果左码右物并且移动了游码,称得溶质质量会偏小,用量筒向烧杯内加液体时要使液体沿着烧杯壁慢慢流下,防止液体溅出,否则水少了,溶质质量分数偏大;
(3)根据图示很明显看出称量和溶解的步骤;氯化钠质量=100g×12%=12g,氯化钠中含有少量不溶的杂质,会导致氯化钠质量偏小,溶质质量分数偏小,量筒量程的选取方法是比所量液体多,并最接近的.
故答案为:(1)烧杯;玻璃棒;(2)氯化钠和砝码位置放反,造成称量不准(或量筒中的水没有沿烧杯内壁倒入,造成液滴飞溅);(3)称量;溶解;12
(2)应该左物右码,如果左码右物并且移动了游码,称得溶质质量会偏小,用量筒向烧杯内加液体时要使液体沿着烧杯壁慢慢流下,防止液体溅出,否则水少了,溶质质量分数偏大;
(3)根据图示很明显看出称量和溶解的步骤;氯化钠质量=100g×12%=12g,氯化钠中含有少量不溶的杂质,会导致氯化钠质量偏小,溶质质量分数偏小,量筒量程的选取方法是比所量液体多,并最接近的.
故答案为:(1)烧杯;玻璃棒;(2)氯化钠和砝码位置放反,造成称量不准(或量筒中的水没有沿烧杯内壁倒入,造成液滴飞溅);(3)称量;溶解;12
点评:通过回答本题知道了配制溶液所用的基本仪器和操作步骤和实验注意事项,并能灵活分析测量结果.

练习册系列答案
相关题目






