题目内容
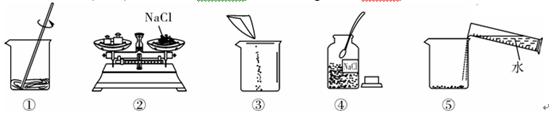
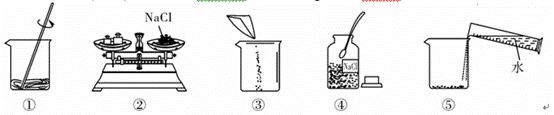
下列是小明同学配制100 g 10% NaCl溶液的实验操作示意图。

(1)该实验正确的操作顺序是________(填序号)。
(2)认真观察指出图中错误的操作步骤________(填序号)。
(3)配制该溶液需要NaCl固体________g,需要水________mL(ρ水=1 g/mL)。
(4)小明同学将称量完毕的食盐转移到烧杯里时,不慎将少量食盐洒落在桌面上,这样会使所配制的溶液中溶质质量分数________10%。(填“>”“=”或“<”)
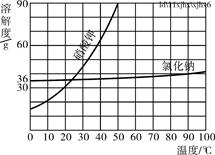
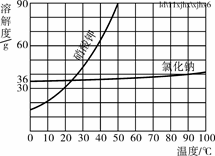
(5)部分物质溶解度曲线如下图所示,在20 ℃时,将40 g NaCl固体加入到100 g水中,搅拌使其充分溶解,你认为所得NaCl溶液的质量是________g,溶质质量分数是________%(精确到0.1%)。

答案 :(1)④②③⑤① (2)② (3)10 90 (4)< (5)136 26.5
:(1)④②③⑤① (2)② (3)10 90 (4)< (5)136 26.5
解析:(1)配制溶液的操作应按计算、称量(固体溶质)、量取(水)、溶解顺序进行;(2)②中称量物质时,将称量物和砝码放反了,应“左物右码”;(3)需要NaCl的质量=100 g×10%=10 g,水的质量为100 g-10 g=90 g,体积为90 g÷1 g/mL=90 mL;(4)因溶解的食盐量减少了,故所配制的溶液中溶质质量分数会变小;(5)查溶解度曲线,20 ℃时NaCl的溶解度为36 g,因此40 g NaCl固体加入到100 g水中,不能全部溶解,最多只能溶解36 g,故所得NaCl溶液的质量是100 g+36 g=136 g,NaCl溶液的溶质质量分数为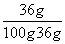 ×100%≈26.5%。
×100%≈26.5%。

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目