题目内容
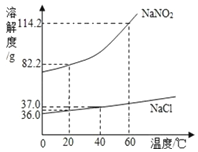
【题目】亚硝酸钠(NaNO2)有毒、有咸味,外形与食盐相似。人若误食会引起中毒NaNO2、NaCl 的溶解度曲线如图所示。请回答下列问题:
(1)某同学设计的鉴别 NaNO2、NaCl 固体的方案如下:
20℃时,取 6.0g NaNO2 和 6.0g NaCl 分别放入两只小烧杯中,各加入 10mL 水(水的密度为 1g/mL)。用玻璃棒充分搅拌后 观察现象。你认为此方案______(填“可行”或“不可行”)。
(2)除去 NaNO2 固体中混有的少量 NaCl,实验步骤,加 水溶解,蒸发浓缩,______,然后过滤、洗涤、干燥。
(3)20℃时,将 182.2g NaNO2 饱和溶液蒸发掉 50g 水,再降温到 20℃,可析出晶体的 质量为______。
(4)根据溶解度曲线,关于 NaNO2 和 NaCl 下列说法中错误的是______。
A 60℃时,NaNO2 溶液的溶质质量分数大于 NaCl 溶液的溶质质量分数
B 20℃时,等质量的两种固体加水配成饱和溶液,所得溶液的质量 NaNO2 溶液大于 NaCl溶液
C 40℃时,NaNO2 的饱和溶液降低温度,溶质质量分数减少
D 60℃时,两种物质的饱和溶液降温到 20℃时,NaNO2 析出的晶体较多
【答案】可行 降温结晶 41.1g A
【解析】
(1)20℃时亚硝酸钠的溶解度是82.2g,即100g水中最多溶解82,2g的亚硝酸钠,而氯化钠的溶解度是37.0g;故取6.0gNaNO2和6.0gNaCl分别放入两只小烧杯中,各加入10mL水(水的密度为1g/mL)。用玻璃棒充分搅拌后,亚硝酸钠可完全溶解,氯化钠最多溶解3.7g;所以观察现象:全部溶解的是NaNO2,有剩余固体的是氯化钠,因此该方案可行;
(2)根据题目信息和溶解度曲线可知:NaNO2、NaCl两种固体物质的溶解度,都是随温度升高而增大,而NaNO2溶解度随温度的升高变化比NaCl的大,而氯化钠的溶解度随温度升高变化不大;所以除去NaNO2固体中混有的少量NaCl,可加水溶解,蒸发浓缩,降温结晶,然后过滤、洗涤、干燥即可;
(3)20℃时NaNO2的溶解度为82.2g,即100g水中最多溶解82.2g的亚硝酸钠,将182.2gNaNO2饱和溶液蒸发掉50g水,再降温到20℃,溶液中最多溶解41.1g,可析出晶体的质量是41.1g;
(4)A.60℃时,NaNO2的溶解度大于NaCl的溶解度,则溶液的溶质质量分数大于NaCl溶液的溶质质量分数,故说法正确。
B.20℃时,等质量的两种固体加水配成饱和溶液,所得溶液的质量NaNO2溶液小于NaCl溶液,故说法错误。
C.40℃时,NaNO2的饱和溶液降低温度,该物质的溶解度减小,则溶质质量分数减少,故说法正确。
D.NaNO2溶解度随温度的升高变化比NaCl的大,则60℃时,两种物质的饱和溶液降温到20℃时,NaNO2析出的晶体较多,故说法正确。
故答案为:(1)可行;(2)降温结晶;(3)41.1g;(4)A。

 阅读快车系列答案
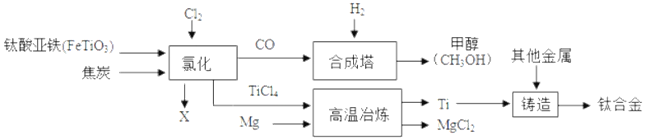
阅读快车系列答案【题目】海水晒盐可制得粗盐,粗盐除氯化钠外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质,以下是某化学兴趣小组制定的一套制备精盐的实验方案,步骤如图所示:
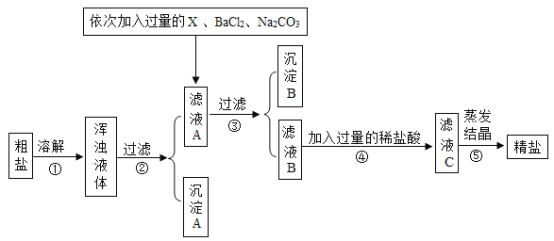
(查阅资料)可溶性钡盐有剧毒,可以导致蛋白质变性,破坏体内一系列生理活动。
(1)步骤①中溶解粗盐时所加水的质量不宜过多,也不宜过少,过少会造成精盐的产率_____(填“偏高”或“偏低”)。沉淀B中共有_____种物质。
(2)符合试剂X要求的是_____(选填字母)。
A 碳酸钙
B 氢氧化钡溶液
C 氢氧化钠溶液
D 氢氧化钙溶液 E 氢氧化钾溶液
(3)甲乙同学为了证明滤液C是否有盐酸剩余,设计了下列实验方法进行实验探究。
(实验探究)
实验 | 实验操作 | 实验现象 | 实验结论 |
甲 | 取样,加入足量AgNO3溶液。 | _____ | 盐酸有剩余。写出盐酸发生反应的化学方程式_____。 |
乙 | 取样,加入适量的_____溶液。 | 有气泡逸出 | 盐酸有剩余。 |
丙同学认为甲的实验方案不严密,请说出理由_____。