题目内容
【题目】某化学拓展课堂的主题是:探秘氯化钠样品。
主题Ⅰ 探究氯化钠样品中杂质的成分
已知所提供的氯化钠样品中,可能含有硫酸钠、氯化镁、氯化钙中的一种或几种杂质。甲同学的实验探究过程记录如下:
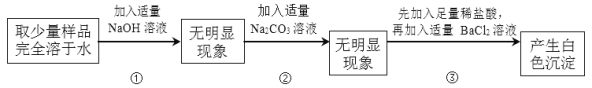
根据以上实验信息,甲同学得出结论:此氯化钠样品中含有的杂质是硫酸钠。
(实验分析)
(1)步骤①中加入适量NaOH 溶液的目的是_____。
(2)乙同学认为步骤③中不需要加入足量稀盐酸,你是否同意他的观点?_____(选填“同意”或“不同意”),请说明原因_________。
主题Ⅱ 测定氯化钠样品中氯化钠的质量分数
确定了氯化钠样品中杂质的成分后,甲同学对样品中氯化钠的质量分数进行测定。称取20.0g 氯化钠样品于烧杯中,加足量的水充分溶解,再向其中加入氯化钡溶液至不再产生沉淀为止,沉淀经过滤、洗涤、干燥后称量,其质量为 2.33g。该样品中氯化钠的质量分数是_____。(写出计算步骤,计算结果精确到 0.1%)
【答案】判断杂质中是否含有氯化镁 不同意 加入稀盐酸要排除碳酸钠的干扰 92.9%
【解析】
氢氧化钠和氯化镁反应生成氯化钠和氢氧化镁白色沉淀,无明显现象,说明不含氯化镁,加入碳酸钠溶液,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,无明显现象,说明不含氯化钙,加入氯化钡溶液生成白色沉淀,说明含有硫酸钠。
(1)氢氧化钠和氯化镁反应生成氯化钠和氢氧化镁白色沉淀,故步骤①中加入适量NaOH 溶液的目的是判断杂质中是否含有氯化镁。
(2)乙同学认为步骤③中不需要加入足量稀盐酸,不同意他的观点,原因是碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,加入稀盐酸要排除碳酸钠的干扰。
称取20.0g 氯化钠样品于烧杯中,加足量的水充分溶解,再向其中加入氯化钡溶液至不再产生沉淀为止,沉淀经过滤、洗涤、干燥后称量,其质量为2.33g,则生成的硫酸钡的质量为2.33g,设样品中硫酸钠的质量为x
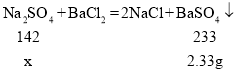
![]()
![]()
该样品中氯化钠的质量分数是![]()

 百年学典课时学练测系列答案
百年学典课时学练测系列答案【题目】元素周期表是学习化学的重要工具。下表中列出了部分元素的原子序数,回答下列问题:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
第一周期 | 1 | 2 | ||||||
第二周期 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
第三周期 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | Ar |
(1)表中铝元素原子的核内质子数为________。
(2)18号元素的原子结构示意图为________。
(3)9号和12号元素形成的化合物的化学式为________。
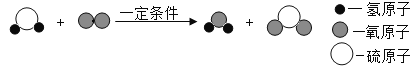
(4)下图是某化学反应的微观示意图,该反应的化学方程式为________。