题目内容
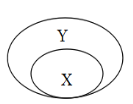
【题目】在化学复习课上,同学们对酸的化学性质进行了梳理和概括,并用下图表达了他们的研究成果。请你根据图回答下列问题。
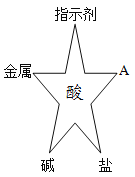
(1)A的物质类别属于_____。
(2)不同的酸有相似的化学性质是因为不同的酸溶液中都含有_____(填微粒符号)。
(3)根据酸和碱的反应,可用氢氧化铝治疗胃酸过多,其化学方程式为______________。
(4)下列反应中没有体现酸的通性的是__________(填序号)。
①稀硫酸和氯化钡溶液反应②稀硫酸和碳酸钠溶液反应
【答案】金属氧化物 H+ Al(OH)3+3HCl=AlCl3+3H2O ①
【解析】
(1)酸可以与指示剂、金属、金属氧化物、碱、盐反应,所以A类物质为金属氧化物;
(2)在水溶液中电离出的阳离子全部是氢离子的化合物是酸,所以酸溶液中都含有H+;
(3)氢氧化铝和盐酸反应生成氯化铝和水,其化学方程式为Al(OH)3+3HCl=AlCl3+3H2O;
(4)①稀硫酸和氯化钡溶液产生沉淀硫酸钡,不是氢离子参与的,不能体现酸的通性,故不属于酸的通性;
②碳酸钠溶液和稀硫酸相互交换成分有硫酸钠、水和二氧化碳,能发生反应,而且是氢离子的参与的反应,故属于酸的通性。

练习册系列答案
相关题目
【题目】某兴趣小组对石灰石样品进行如下实验取 12g 样品放入烧杯中,将 100g 稀盐酸分 4 次加入到烧杯中,充分反应后(杂质不溶于水,也不与酸反应),测得剩余固体的质量记录如下。请计算:
次数 | 1 | 2 | 3 | 4 |
加入稀盐酸的质量/g | 25 | 25 | 25 | 25 |
剩余固体的质量/g | 8 | 4 | 2 | 2 |
求:第 4 次加入稀盐酸后所得溶液中 CaCl2的质量分数。(写出计算过程,最终结果保留 0.1%)。