题目内容
【题目】热水瓶用久后瓶胆内壁常附着一层水垢,其成分是碳酸钙、氢氧化镁.实验室现有一瓶水垢样品,为测定其中各成分的质量分数,某化学兴趣小组的同学利用如图所示装置进行实验(该装置气密性良好,A、C、D中所装药品足量).已知:碱石灰是氧化钙和氢氧化钠的固体混合物,在高温的条件下,氢氧化镁也发生分解,生成氧化镁和水蒸气.
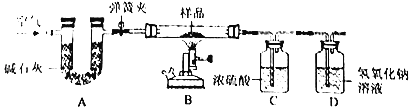
部分实验步骤如下:①将质量为m的水垢样品装入装置B的玻璃管中,按图连接好装置,关闭弹簧夹,给样品加热;②待样品完全反应,先打开弹簧夹通入空气,再熄灭酒精喷灯,直到玻璃管冷却;③实验完毕,测得装置C、D中的液体质量分别增加了m1、m2,并计算水垢中各成分的质量分数.
则下列说法正确的是( )
A. B装置中发生反应的基本类型是分解反应
B. m2是样品完全反应后产生的二氧化碳的质量
C. 若没有装置A,会导致氢氧化镁的测定结果偏小
D. 若装置C和装置D位置颠倒,不会影响碳酸钙的测定结果
【答案】A
【解析】装置C、D中的液体增加的质量分别是吸收的水和二氧化碳的质量。A. B装置中发生的反应:CaCO3高温CaO+CO2↑,Mg(OH)2![]() MgO + H2O,由一种物质生成两种物质的反应属于分解反应,正确;B. 由于通入的空气中含有二氧化碳,故m2大于样品完全反应后产生的二氧化碳的质量,错误;C. 若没有装置A,空气中的水蒸气也进入装置C,会导致氢氧化镁的测定结果偏大,错误;D. 若装置C和装置D位置颠倒,装置D增加的质量大于生成二氧化碳的质量,会影响碳酸钙的测定结果,错误。故选A。
MgO + H2O,由一种物质生成两种物质的反应属于分解反应,正确;B. 由于通入的空气中含有二氧化碳,故m2大于样品完全反应后产生的二氧化碳的质量,错误;C. 若没有装置A,空气中的水蒸气也进入装置C,会导致氢氧化镁的测定结果偏大,错误;D. 若装置C和装置D位置颠倒,装置D增加的质量大于生成二氧化碳的质量,会影响碳酸钙的测定结果,错误。故选A。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目