题目内容
8、(1)20世纪初,丹麦和英国的一些科学家提出了新的酸碱理论--质子论.质子论认为:凡能放出质子(即H+)的分子或离子都是酸,凡能结合质子的分子或离子都是碱.根据这个理论,试判断:①H2SO4 ②OH- ③H2PO4- ④NO3- ⑤Al3+ 中属于酸的是(填序号,下同)
(2)下表是几种常见气体单质的物理常数:
从这些物理常数中你能总结出非金属气体单质沸点、密度、溶解度的变化规律吗?
①
②
③
由此可见,非金属气体单质的物理性质与其
(3)如下图所示,往试管中放入几小块生石灰,然后把试管放在盛有25℃时的饱和石灰水的烧杯中,再用滴管滴入5mL蒸馏水.

试回答下列问题:
实验时观察到烧杯中出现的现象为
①和③
,属于碱的是②、③、④
.(2)下表是几种常见气体单质的物理常数:
| 物理常数 | H2 | N2 | O2 | Cl2 |
| 0℃时的溶解度 | 1.92 | 29.4 | 69.5 | 1460 |
| 密度(g/L) | 0.0899 | 1.2506 | 1.429 | 3.214 |
| 熔点(℃) | 259.14 | 209.86 | 218.4 | 100.98 |
| 沸点(℃) | 252.4 | 195.8 | 182.96 | 34.6 |
①
沸点随相对分子质量增加而升高
;②
密度随相对分子质量增加而增大
;③
溶解度随相对分子质量增加而增大
;由此可见,非金属气体单质的物理性质与其
相对分子质量
有关.(3)如下图所示,往试管中放入几小块生石灰,然后把试管放在盛有25℃时的饱和石灰水的烧杯中,再用滴管滴入5mL蒸馏水.

试回答下列问题:
实验时观察到烧杯中出现的现象为
生石灰遇水放出大量热,饱和石灰水变浑浊
;产生上述现象的原因是生石灰遇水放出大量热,使饱和石灰水温度升高;
,Ca(OH)2的溶解度随温度升高而减小
,Ca(OH)2从饱和溶液中析出
.分析:(1)(1)根据质子论对给出的物质进行分析,凡是能电离出H+的分子或离子都属于酸,凡是能结合H+的分子或离子都属于碱.特别注意某些离子既能放出H+又能结合H+的既属于酸又属于碱;
(2)首先分析给出非金属气体单质排列规律,再分析、比较沸点、密度、溶解度的变化规律;
(3)根据生石灰和水反应生成氢氧化钙,放出大量的热,Ca(OH)2的溶解度随温度升高而减小分析现象和原因.
(2)首先分析给出非金属气体单质排列规律,再分析、比较沸点、密度、溶解度的变化规律;
(3)根据生石灰和水反应生成氢氧化钙,放出大量的热,Ca(OH)2的溶解度随温度升高而减小分析现象和原因.
解答:解:(1)硫酸能解离出H+,属于酸;OH-能结合H+生成水,属于碱;HCO3-能解离出H+和碳酸根离子,属于酸,同时又能结合H+生成碳酸,所以又属于碱;NO3-能结合H+生成硝酸,所以属于碱;Al3+既不能结合H+又不能放出H+,所以既不属于酸又不属于碱,所以,属于酸的是①和③,属于碱的是②、③、④;
(2)通过比较H2、N2、O2、Cl2相对分子质量可以看出,它们的相对分子质量逐渐增大,再分析、比较沸点、密度、溶解度的变化规律发现:①沸点随相对分子质量增加而升高,②密度随相对分子质量增加而增大,③溶解度随相对分子质量增加而增大,由此可见,非金属气体单质的物理性质与其相对分子质量有关;
(3)向生石灰滴入蒸馏水时,生石灰和水反应生成氢氧化钙,放出大量的热,使饱和的石灰水温度升高,
Ca(OH)2的溶解度随温度升高而减小,Ca(OH)2从饱和溶液中析出,饱和的石灰水变浑浊.
故答为:(1)①和③,②、③、④;
(2)①沸点随相对分子质量增加而升高,②密度随相对分子质量增加而增大,③溶解度随相对分子质量增加而增大,相对分子质量;
(3)生石灰遇水放出大量热,饱和石灰水变浑浊,生石灰遇水放出大量热,使饱和的石灰水温度升高,Ca(OH)2的溶解度随温度升高而减小,Ca(OH)2从饱和溶液中析出.
(2)通过比较H2、N2、O2、Cl2相对分子质量可以看出,它们的相对分子质量逐渐增大,再分析、比较沸点、密度、溶解度的变化规律发现:①沸点随相对分子质量增加而升高,②密度随相对分子质量增加而增大,③溶解度随相对分子质量增加而增大,由此可见,非金属气体单质的物理性质与其相对分子质量有关;
(3)向生石灰滴入蒸馏水时,生石灰和水反应生成氢氧化钙,放出大量的热,使饱和的石灰水温度升高,
Ca(OH)2的溶解度随温度升高而减小,Ca(OH)2从饱和溶液中析出,饱和的石灰水变浑浊.
故答为:(1)①和③,②、③、④;
(2)①沸点随相对分子质量增加而升高,②密度随相对分子质量增加而增大,③溶解度随相对分子质量增加而增大,相对分子质量;
(3)生石灰遇水放出大量热,饱和石灰水变浑浊,生石灰遇水放出大量热,使饱和的石灰水温度升高,Ca(OH)2的溶解度随温度升高而减小,Ca(OH)2从饱和溶液中析出.
点评:本题要求我们利用题中所给出的质子论,对初中化学在酸、碱的认识基础上,从新的理论角度分析酸和碱,注意范围扩展到分子或离子范围,同时又要注意根据新的理论有些物质既属于酸又属于碱.

练习册系列答案
相关题目
(1)20世纪初,丹麦和英国的一些科学家提出了新的酸碱理论--质子论.质子论认为:凡能放出质子(即H+)的分子或离子都是酸,凡能结合质子的分子或离子都是碱.根据这个理论,试判断:①H2SO4 ②OH- ③H2PO4- ④NO3- ⑤Al3+ 中属于酸的是(填序号,下同)______,属于碱的是______.
(2)下表是几种常见气体单质的物理常数:
| 物理常数 | H2 | N2 | O2 | Cl2 |
| 0℃时的溶解度 | 1.92 | 29.4 | 69.5 | 1460 |
| 密度(g/L) | 0.0899 | 1.2506 | 1.429 | 3.214 |
| 熔点(℃) | 259.14 | 209.86 | 218.4 | 100.98 |
| 沸点(℃) | 252.4 | 195.8 | 182.96 | 34.6 |
①______;
②______;
③______;
由此可见,非金属气体单质的物理性质与其______有关.
(3)如下图所示,往试管中放入几小块生石灰,然后把试管放在盛有25℃时的饱和石灰水的烧杯中,再用滴管滴入5mL蒸馏水.
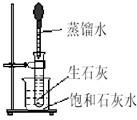
试回答下列问题:
实验时观察到烧杯中出现的现象为______;产生上述现象的原因是______,______,______.
(1)20世纪初,丹麦和英国的一些科学家提出了新的酸碱理论--质子论.质子论认为:凡能放出质子(即H+)的分子或离子都是酸,凡能结合质子的分子或离子都是碱.根据这个理论,试判断:①H2SO4 ②OH- ③H2PO4- ④NO3- ⑤Al3+ 中属于酸的是(填序号,下同) ,属于碱的是 .
(2)下表是几种常见气体单质的物理常数:
从这些物理常数中你能总结出非金属气体单质沸点、密度、溶解度的变化规律吗?
① ;
② ;
③ ;
由此可见,非金属气体单质的物理性质与其 有关.
(3)如下图所示,往试管中放入几小块生石灰,然后把试管放在盛有25℃时的饱和石灰水的烧杯中,再用滴管滴入5mL蒸馏水.
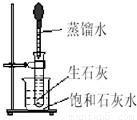
试回答下列问题:
实验时观察到烧杯中出现的现象为 ;产生上述现象的原因是 , , .
(2)下表是几种常见气体单质的物理常数:
| 物理常数 | H2 | N2 | O2 | Cl2 |
| 0℃时的溶解度 | 1.92 | 29.4 | 69.5 | 1460 |
| 密度(g/L) | 0.0899 | 1.2506 | 1.429 | 3.214 |
| 熔点(℃) | 259.14 | 209.86 | 218.4 | 100.98 |
| 沸点(℃) | 252.4 | 195.8 | 182.96 | 34.6 |
① ;
② ;
③ ;
由此可见,非金属气体单质的物理性质与其 有关.
(3)如下图所示,往试管中放入几小块生石灰,然后把试管放在盛有25℃时的饱和石灰水的烧杯中,再用滴管滴入5mL蒸馏水.

试回答下列问题:
实验时观察到烧杯中出现的现象为 ;产生上述现象的原因是 , , .