题目内容
有机物A在氧气中燃烧后只生成二氧化碳和水,为确定A的组成,某同学进行了如下探究.【猜想】
猜想一:A中只含C、H两种元素
猜想二:A中含C、H、O三种元素
【实验】

【结论】猜想______正确(选填“一”或“二”).
【反思】有机物A中所含元素的原子个数比为______.
【答案】分析:根据物质燃烧后生成的水中的氢元素和二氧化碳中的碳元素都是来自于该物质,将碳元素的质量加上氢元素的质量如果等于3.1g就没有氧元素,如果小于3.1g就含有氧元素;含有氧元素的质量就是用3.1g-碳元素质量-氢元素的质量.
解答:解:根据质量守恒定律可知,物质燃烧后生成的水中的氢元素和二氧化碳中的碳元素都是来自于该物质,所以物质中的氢元素质量为:2.7g× ×100%=0.3g,物质中的碳元素质量为:4.4g×
×100%=0.3g,物质中的碳元素质量为:4.4g× ×100%=1.2g,所以物质中的氧元素为:3.1g-0.3g-1.2g=1.6,所以有机物A中所含元素的原子个数比为C:H:O=
×100%=1.2g,所以物质中的氧元素为:3.1g-0.3g-1.2g=1.6,所以有机物A中所含元素的原子个数比为C:H:O=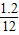 :
: :
: =1:3:1
=1:3:1
故答案为:二;1:3:1
点评:本题主要考查学生运用质量守恒定律解答问题的能力.运用质量守恒定律判断物质中含有的元素,是有关质量守恒定律的题目中常见的类型,解题的关键是正确理解质量守恒定律关于反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变.
解答:解:根据质量守恒定律可知,物质燃烧后生成的水中的氢元素和二氧化碳中的碳元素都是来自于该物质,所以物质中的氢元素质量为:2.7g×
 ×100%=0.3g,物质中的碳元素质量为:4.4g×
×100%=0.3g,物质中的碳元素质量为:4.4g× ×100%=1.2g,所以物质中的氧元素为:3.1g-0.3g-1.2g=1.6,所以有机物A中所含元素的原子个数比为C:H:O=
×100%=1.2g,所以物质中的氧元素为:3.1g-0.3g-1.2g=1.6,所以有机物A中所含元素的原子个数比为C:H:O=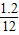 :
: :
: =1:3:1
=1:3:1故答案为:二;1:3:1
点评:本题主要考查学生运用质量守恒定律解答问题的能力.运用质量守恒定律判断物质中含有的元素,是有关质量守恒定律的题目中常见的类型,解题的关键是正确理解质量守恒定律关于反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案
相关题目
 水是人类最宝贵的自然资源,多一滴水,就可能多一条生命.
水是人类最宝贵的自然资源,多一滴水,就可能多一条生命.



