题目内容
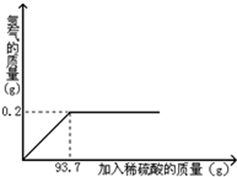
某实验室用30克氯酸钾和5克二氧化锰的混合物加热制取氧气,反应一段时间后,冷却称量,得到25.4g剩余固体物质。试计算:
①生成氧气的物质的量为 摩尔。
②参加反应的氯酸钾的物质的量为 摩尔。(根据化学方程式列式计算)
① 0.3 ② 0.2
解析试题分析:根据质量守恒定律,化学反应前后的质量相等,可直接得出生成氧气的质量=30克+5克-25.4克=9.6克,所以生成氧气的物质的量=9.6g/32g/mol=0.32mol,再根据化学方程式:2KClO3 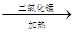 2KCl+3O2↑中KClO3和O2的质量关系,即可求出氯酸钾的物质的量
2KCl+3O2↑中KClO3和O2的质量关系,即可求出氯酸钾的物质的量
解:设参加反应的氯酸钾的物质的量为x
2KClO3 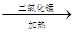 2KCl+3O2↑
2KCl+3O2↑
2 3
xmol 0.3mol
2/x =3/0.3
x=0.2(mol)
考点:质量守恒定律的应用,根据化学方程式进行的计算

我国约在南北朝时就开始冶炼黄铜。黄铜是铜和锌的合金(Cu-Zn),它可用来制造机器、电器零件及日用品。为了测定某黄铜样品中锌的质量分数(不考虑黄铜中的其他杂质),现将15 mL稀盐酸分三次加入到5 g黄铜样品粉末中,每次充分反应后,测定生成氢气的质量,实验数据见下表:
| | 第一次 | 第二次 | 第三次 |
| 加入稀盐酸的体积(mL) | 5 | 5 | 5 |
| 生成氢气的质量(g) | 0.04 | m | 0.02 |
试求:(1)m=________________;
(2)此黄铜样品中锌的质量分数是多少?
为了测定某牛奶样品中蛋白质的含量,现采用“盖尔达法”分解其中的蛋白质。其原理是把蛋白质中的氮元素完全转化成氨气(化学式为NH3),再用稀硫酸吸收氨气,反应的化学方程式:2NH3+H2SO4=(NH4)2SO4
现取该牛奶样品30 mL,用“盖尔达法”分解其中的蛋白质,产生的氨气用9.5 g溶质质量分数为4.9%的稀硫酸恰好完全吸收。计算并回答下列问题:
(1)产生氨气的质量是多少克?(计算结果精确到0.01 g,下同)
(2)30 mL牛奶中含氮元素的质量是多少克?
(3)下图是该牛奶包装标签的部分内容。已知牛奶中的蛋白质含氮元素的质量分数为16%,请你通过计算确定,该牛奶样品中蛋白质的含量是否达到了包装标签所标示的蛋白质的质量标准。
| 配料:鲜牛奶 保质期:8个月 净含量:250 mL/盒 营养成分:(每100 mL) 钙≥0.11 g 脂肪≥3.30 g 蛋白质≥2.90 g |