题目内容
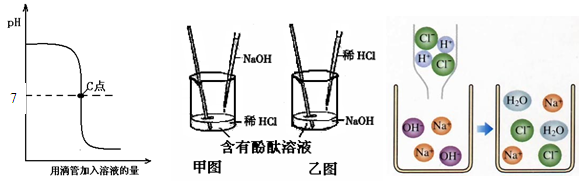
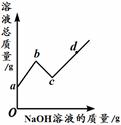
向一定量硫酸和硫酸铜的混合溶液中,逐滴加入一定质量分数的氢氧化钠溶液,直至过量。某同学依据实验事实绘制了如图所示的曲线。下列说法正确的是 ( )

| A.a至b段对应溶液的pH逐渐减小 |
| B.b点对应溶液中的溶质为硫酸钠 |
| C.c点对应溶液中的溶质种类最少 |
| D.a至d段硫酸钠的质量逐渐增大 |
C
试题分析:有题中图像可知A选项a至b段对应溶液的pH逐渐减小是错误的叙述,酸碱中和溶液的pH值增大;B选项是错误的叙述,b点时溶液中的溶质为硫酸钠和硫酸铜;C选项c点时氢氧化钠和硫酸铜反应完全,溶液中的溶质为硫酸钠;D选项是错误的叙述,在c—d段硫酸钠的质量不变,故答案选选择C

练习册系列答案
相关题目