题目内容
7、以氢氧化钠溶液为例,归纳小结碱的共同性质.填写下表: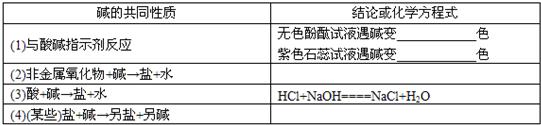

分析:根据碱类物质的反应规律,结合氢氧化钠的性质,举例说明碱与其他物质反应的事实.
解答:解:(1)无色酚酞试液遇酸或中性溶液不变色,而遇碱性溶液变红色;紫色石蕊试液遇酸性溶液变红色,遇碱性溶液变蓝色,遇中性溶液不变色仍为紫色;
故答案为:红;蓝;
(2)这里的“非金属氧化物”通常指CO2、SO2、SO3,碱应为可溶性碱;
故答案为:2NaOH+SO2=Na2SO3+H2O;
(4)“某些盐”通常指盐本身可溶,且盐中的金属离子与氢氧根离子结合生成沉淀或盐中的酸根离子与碱中的金属离子结合生成沉淀.
故选CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.
故答案为:红;蓝;
(2)这里的“非金属氧化物”通常指CO2、SO2、SO3,碱应为可溶性碱;
故答案为:2NaOH+SO2=Na2SO3+H2O;
(4)“某些盐”通常指盐本身可溶,且盐中的金属离子与氢氧根离子结合生成沉淀或盐中的酸根离子与碱中的金属离子结合生成沉淀.
故选CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.
点评:非金属氧化物与碱溶液的反应,虽然与两种化合物反应生成另两种化合物,但却因没有交换成分,所以此类反应不属于复分解反应.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
以氢氧化钠溶液为例,归纳小结碱的共同性质.填写下表:
| 碱的共同性质 | 结论或化学性质 |
| (1)与酸碱指示剂的反应 | 无色酚酞试液遇碱变_________色 紫色石蕊试液遇碱变_________色 |
| (2)非金属氧化物+碱→盐+水 | |
| (3)酸+碱→盐+水 | HCl+NaOH=NaCl+H2O |
| (4)(某些)盐+碱→另盐+另碱 |
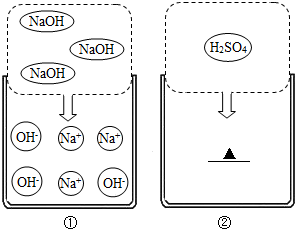
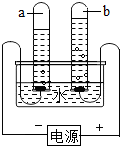
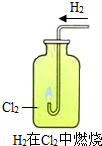



 2HCl.
2HCl.


 2HCl.
2HCl.