题目内容
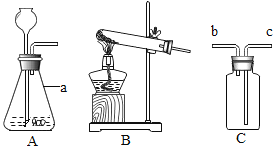
【题目】硫化氢(H2S)是一种有毒气体,其密度比空气大,且能溶于水形成氢硫酸。实验室通常用块状固体硫化亚铁(FeS)与稀硫酸混合,在常温下通过发生复发解反应制得硫化氢气体。试回答:

(1)实验室制取硫化氢气体的化学方程式为_________。
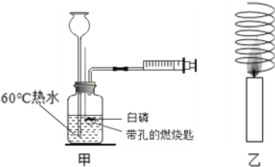
(2)制取硫化氢气体的发生装置可选用_____________。
(3)若用C装置收集硫化氢气体,进气口应为______,原因是______________。
(4)为了验证硫化氢的水溶液呈酸性,可将该气体通入装置D,D中所盛试剂应该是______,现象是______。
(5)做上述实验时,为了防止多余的硫化氢逸出污染环境,可将其通入装置E吸收,E中试剂为________溶液。
【答案】FeS+H2SO4=FeSO4+H2S↑ B b 硫化氢气体的密度比空气大 紫色石蕊试液 溶液由紫色变成红色 氢氧化钠
【解析】
(1)硫化亚铁(FeS)与稀硫酸反应生成硫酸亚铁和硫化氢气体;故填:FeS+H2SO4=FeSO4+H2S↑。
(2)实验室通常用块状固体硫化亚铁(FeS)与稀硫酸混合,在常温下通过发生复发解反应制得硫化氢气体,因此不需要加热,所以发生装置选用B。故填:B。
(3)若用C装置收集硫化氢气体,进气口应为长管,因为硫化氢气体的密度比空气大,故答填:b;硫化氢气体的密度比空气大。
(4)可以用紫色石蕊试液验证硫化氢的水溶液呈酸性,可将该气体通入石蕊试液中,紫色变红色就证明硫化氢气体显酸性;故填:紫色石蕊试液;溶液由紫色变成红色。
(5)氢氧化钠溶液可以与硫化氢气体反应,因此可用它吸收硫化氢气体,防止空气污染,故填:氢氧化钠。

【题目】某研究小组在学习氧气的化学性质时发现:铁丝在氧气中燃烧没有火焰,而蜡烛在氧气中燃烧却有明亮的火焰。该小组同学进行了如下探究。
(1)写出铁丝在氧气中燃烧的符号表达式:_____。
(2)探究一:蜡烛燃烧产生火焰的原因是什么?
点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生。由此可知:蜡烛燃烧产生的火焰是由_____(填“固态”或“气态”)物质燃烧形成的。
(3)探究二:物质燃烧产生火焰的根本原因是什么?
物质 | 熔点╱℃ | 沸点╱℃ | 燃烧时温度╱℃ |
石蜡 | 50∽70 | 300∽550 | 约600 |
铁 | 1535 | 2750 | 约1800 |
钠 | 97.8 | 883 | 约1400 |
由上表可知:物质燃烧能否产生火焰与其_____(填“熔点”或“沸点”)和燃烧时温度有关。通过上表中石蜡、铁的数据对比,你认为物质燃烧时,什么情况下能产生火焰_____。由此推测:钠在燃烧时,_____(填“有”或“没有”)火焰产生。