题目内容
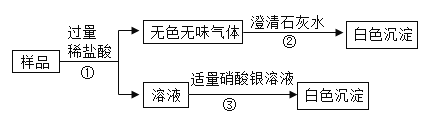
【题目】现有Na2CO3、NaHCO3的混合物19.0g,加热充分反应,至固体质量不再减少,剩余固体的质量为15.9g,则下列判断中,正确的是
A.混合物加热发生了分解反应
B.剩余固体是纯净物
C.原混合物中Na2CO3的质量为10.6g
D.反应产生二氧化碳的质量为6.6g
【答案】ABC
【解析】
碳酸氢钠加热生成碳酸钠、水和二氧化碳。
A、碳酸氢钠加热生成碳酸钠、水和二氧化碳,反应符合一变多,属于分解反应,则混合物加热发生了分解反应,故A正确;
B、碳酸氢钠加热生成碳酸钠、水和二氧化碳,剩余固体是碳酸钠,属于纯净物,故B正确;
C、设分解的碳酸氢钠的质量为x
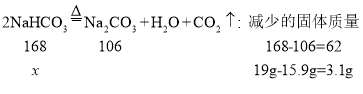
![]()
![]()
原混合物中Na2CO3的质量为![]() ,故C正确;
,故C正确;
D、设碳酸氢钠分解生成的二氧化碳的质量为y
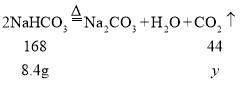
![]()
![]()
反应产生二氧化碳的质量为2.2g,故D不正确。
故选ABC。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目