题目内容
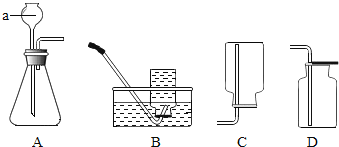
下表是元素周期表的一部分,回答问题:
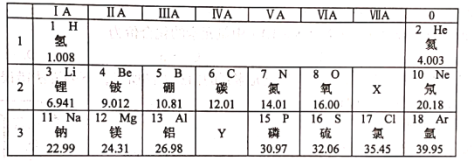
(1)写出X的元素符号_______。
(2)画出元素Y的原子结构示意图_________。
(3)13号元素和17号元素形成的化合物的化学式为_________。
(4)16号元素的原子在化学反应时容易_______(填“得到”或“失去”)电子,形成的简单离子表示为________。
 智能训练练测考系列答案
智能训练练测考系列答案某同学在实验室测定了几种溶液的pH,其结果如下表:
溶液 | 盐酸 | CuCl2溶液 | Na2SO4溶液 | 水 | Na2CO3溶液 | NaOH溶液 |
pH | 1 | 3 | 7 | 7 | 11 | 13 |
该同学由此得出的结论正确的是
A.碳酸钠溶液呈碱性,故属于碱 B.上述CuCl2溶液的酸性比盐酸强
C.盐溶液一定呈中性 D.利用酚酞能区分CuCl2溶液和NaOH溶液
某实验小组将少量氢化钙(CaH2)溶于水,形成了无色透明的溶液,再向其中加入碳酸钠溶液,有沉淀产生,经过滤后得到滤渣和滤液。然后进行了滤渣验证和滤液溶质成分的探究。
(1)(查阅资料)氢化钙在常温下能与水反应生成氢氧化钙和氢气,写出该反应的化学方程式______________。
(2)(交流验证)滤渣只能是碳酸钙,用盐酸验证此滤渣的化学方程式为______________。
(3)(提出问题)滤液中溶质的成分是什么?
(4)(猜想假设)猜想一:NaOH
猜想二:NaOH和Na2CO3
猜想三:NaOH和________。
猜想四:NaOH、Na2CO3和Ca(OH)2
(5)(讨论分析)经过讨论认为最不合理的是猜想____,原因是______________。
(6)(实验与结论)
实验步骤 | 现象 | 结论 |
步骤I:取少量滤液,向其中加入足量盐酸溶液 | ________ | 猜想二不成立 |
步骤Ⅱ:另取少量滤液,向其中滴入适量Na2CO3溶液 | 产生白色沉淀 | 猜想____成立 |
(7)(拓展延伸)在分析反应后所得物质的成分时,除考虑生成物外,还需考虑___________。



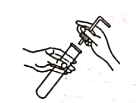 B.滴加液体
B.滴加液体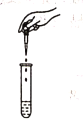
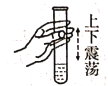 D.倾倒液体
D.倾倒液体