题目内容
【题目】根据图中提供的信息,请回答下列问题:
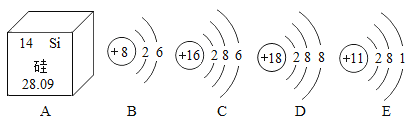
(1)由A图可知,硅的质子数为_____;
(2)B、C、D、E中属于同种元素的是_____;(填字母序号)
(3)B、C元素化学性质相似的原因是_____;
(4)B、E两种元素组成化合物的化学式为_____。
【答案】14 CD 最外层电子数相同 Na2O或者Na2O2
【解析】
(1)A为元素示意图,左上角数字表示原子序数,原子序数=原子核内质子数,所以硅原子的质子数为14;
(2)元素种类由核内质子数决定,相同核内质子数表示同一种元素,C与D核内质子数都为16,所以为同一种元素即硫元素;
(3)元素化学性质由最外层电子数决定,所以元素的化学性质相似是因为核外电子数相同;
(4)由微观结构示意图可知B元素为氧,E元素为钠,钠与氧可以形成氧化钠和过氧化钠两种化合物,所以化学式为Na2O或者Na2O2。

【题目】下列实验操作能达到实验目的是( )
选项 | 实验目的 | 实验操作 |
A | 鉴别木炭粉和铁粉 | 加稀盐酸,观察有无气泡产生 |
B | 鉴别氮气和二氧化碳 | 将燃着的木条分别伸入盛气体的集气瓶中 |
C | 除去一氧化碳中的氧气 | 将气体缓慢通过灼热的铜网 |
D | 除去FeSO4溶液中少量的CuSO4 | 加入足量锌粉,充分反应后过滤 |
A.AB.BC.CD.D
【题目】欲测定铜镁合金的组成(其他元素忽略不计),进行如下实验:取铜镁合金20g放入烧杯,将200g稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量记录如下:
次数 | 1 | 2 | 3 | 4 |
加入稀硫酸质量/g | 50 | 50 | 50 | 50 |
剩余固体质量/g | 17.6 | 15.2 | m | 14 |

(1) m的值是_____,合金中铜、镁的质量最简比是_____。
(2)计算所加稀硫酸的溶质的质量分数_____;( 写出计算过程)
(3)在如图画出加入稀硫酸与产生气体关系的曲线图_____。
【题目】在一定条件下,在一个封闭的容器内发生某反应,测得反应前后各物质的质量如表
物质 | W | O2 | H2O | CO2 |
反应前质量/g | 8 | 20 | 1 | O |
反应后质量/g | 0 | 8 | 10 | a |
下列判断正确的是
A.表中a的值为18
B.W一定含有碳、氢、氧三种元素
C.该反应属于分解反应
D.W和氧气在反应中的质量比为2:5