题目内容
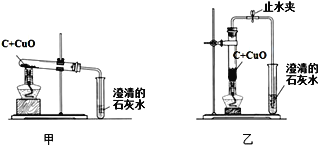
【题目】木炭作为还原剂用于金属冶炼已有几千年历史。化学兴趣小组按照课本实验方法(如图甲),做木炭与氧化铜反应实验时,发现很难观察到紫红色铜的生成,他们决定对这个实验进行探究和改进。
(1)木炭与氧化铜反应的化学方程式是________。
(2)小波建议用超细炭粉与氧化铜粉末混合进行实验,你认为这样建议的原理是_______。
(3)小周建议用图乙装置替代图甲装置。与图甲相比较,图乙装置中将试管直立放置、将反应混合物夯实于试管底部,并通过调节酒精灯可使外焰完全包围试管的下部,这样设计的原因是________。
(4)检查了乙装置的气密性后,往试管中加入已干燥的药品并开始加热,当看到澄清的石灰水刚出现浑浊时,_______(填“可以”或“不能”)确定氧化铜和炭粉已经开始反应。
(5)待反应结束,先将导气管从石灰水中取出,然后关闭止水夹,让产物自然冷却。若不关闭止水夹,可能出现的问题是___。待产物冷却后,同学们终于找到了期待已久的紫红色铜珠,实验获得了圆满成功。
【答案】C+2CuO![]() 2Cu+CO2↑ 增大反应物的接触面积,使反应更充分 使火焰集中,获得持续高温 不能 空气进入试管中,使生成的铜重新被氧化
2Cu+CO2↑ 增大反应物的接触面积,使反应更充分 使火焰集中,获得持续高温 不能 空气进入试管中,使生成的铜重新被氧化
【解析】
(1)熟记碳还原氧化铜的化学反应式;
(2)与反应物的接触面积越大,反应速率越快;
(3)加上灯罩可以使火焰更集中,提升温度;
(4)根据碳也可以与氧气反应生成二氧化碳分析;
(5)根据灼热的氧化铜可能会被氧化分析。
(1)碳还原氧化铜可生成铜和二氧化碳,化学反应式时:2CuO+C![]() 2Cu+CO2↑;
2Cu+CO2↑;
(2)与反应物的接触面积越大,反应速率越快,所以把块状的木炭变成碳粉更利于反应的进行;
(3)加上灯罩可以使火焰更集中,提升温度,利于反应的进行;
(4)实验时首先要检查装置的气密性,当看到澄清的石灰水刚出现浑浊时,可能是炭与氧气反应生成的二氧化碳,故不能判断碳一氧化铜发生了反应;
(5)停止加热后,仍能看到红热现象,并沿试管底部自下而上蔓延,这个现象说明该反应要放出热量,反应结束后要关闭止水夹,防止进入空气,使灼热的铜再被氧化。

【题目】化学与生活密切相关。
(1)每100克巧克力中营养成分的含量如下表。
蛋白质/g | 脂肪/g | 糖类/g | 矿物质/mg | 维生素B/mg | 维生素C/mg | 总能量/千焦 | ||
5 | 32 | 51 | 钙 | 铁 | 磷 | 0.2 | _____ | 2142 |
50 | 4 | 120 | ||||||
①表中2142千焦能量全部来自糖类吗? (填“是”或“不是”)。葡萄糖(C2H12O6)完全烧焦后得到黑色物质,说明葡萄糖含 元素(填元素符号)。
②摄入 元素不足。会导致骨骼疏松,易得佝偻病。铁、磷元素中人体必需微量元素的是 。
③补充维生素C,选择 为宜。(填序号)
A.猪肉 B.青菜 C.纯净水
(2)2017年,扬州电缆助力我国货运飞船“天舟一号”顺利升空。
①电缆内一般是铜芯,外面包有聚乙烯绝缘层。铜属于 ,聚乙烯属于 。(填序号)
A.金属材料 B.合成材料 c.复合材料

②纯铜制作铜芯电缆,主要是因为 。(填序号)
A.密度大 B.色彩鲜艳 C.导电能力强
【题目】不少家庭养观赏鱼,有时会在鱼缸里放点鱼浮灵,可使水中的含氧量迅速增加,能有效提高鱼的成活率,并且有杀菌作用。某小组对鱼浮灵成份及原理进行了相关探究。
(实验1)检验气体
查阅资料1:鱼浮灵化学名称是过氧碳酸钠(xNa2CO3yH2O2),常温下,过氧碳酸钠易溶于水并迅速放出氧气。
实验方案1::在一支试管中加入适量的鱼浮灵,____________(将后续操作及现象补充完整),证明产生的气体是氧气。
(实验2)检验反应后溶液中的溶质成分
猜想假设:猜想1:Na2CO3 猜想2:Na2CO3和NaOH
查阅资料2:用一定溶质质量分数的NaOH和Na2CO3两种溶液进行如下实验。
NaOH溶液 | Na2CO3溶液 | |
滴加酚酞溶液 | 现象 | 现象 |
加入稀盐酸 | 无明显现象 | 现象 |
加入澄清石灰水 | 无明显现象 | 现象 |
加入 1%的CaCl2溶液 | 溶液变浑浊 | 溶液变浑浊 |
加入 0.1%的CaCl2溶液 | 无明显现象 | 溶液变浑浊 |
表中的现象 _______(填序号)为溶液变红色,现象③对应的化学反应方程式为____。
实验方案 2:同学们取实验 1 反应后的溶液于试管中,加入过量_____(填“1%”或“0.1%”)的 CaCl 2 溶液,充分反应后过滤,取少量滤液,向滤液中滴加无色酚酞溶液,观察到滤液呈 _______色,证明猜想 1 正确。
(反思拓展) 根据上述探究可知,保存鱼浮灵时应注意___________。