题目内容
【题目】下图是某锌锰干电池的剖面图。
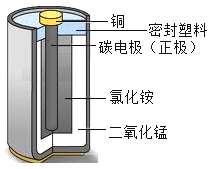
(1)锌锰干电池工作时可以将化学能转化为_________能;
(2)电池中有许多材料,其中属于氧化物的是_______(写化学式);
(3)碳棒具有______性,可作为干电池的电极;
(4)二氧化锰可作为实验室用双氧水制氧气的_______;
(5)废旧电池中的锌可回收利用,用于实验室与稀硫酸反应制取氢气。写出该反应的化学方程式为_______。
【答案】电 MnO2 导电 催化剂 Zn+H2SO4=ZnSO4+H2↑
【解析】
主要涉及到与锌锰干电池相关的一些化学知识点,解题时依据要求对各方面的知识进行分析探讨即可。
(1)干电池的工作原理是电池内部发生化学变化并把化学能转化为电能,故填:电。
(2)氧化物是只含两种元素其中一种元素是氧元素的化合物,干电池中符合要求的是MnO2,故填:MnO2。
(3)作电极的材料一定导电,碳棒也不例外,故填:导电。
(4)在利用双氧水制取氧气的过程中二氧化锰可作催化剂,故填:催化剂;
(5)锌和稀硫酸反应可以制取氢气同时生成硫酸锌,故填:Zn+H2SO4═ZnSO4+H2↑。

【题目】请根据下列装置回答问题:
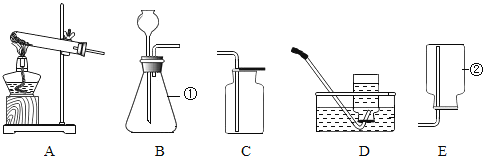
(1)写出①、②的仪器名称:①_____;②_____________。
(2)用字母填写下表
制取的气体 | 发生装置 | 收集装置 |
CO2 | _________ | _________ |
少量的O2 | _________ | D或_________ |
较多的O2 | _________ |
(3)实验室用B装置制取氧气的化学方程式为__________,用D装置收集O2的操作中,当O2收满后接下来要进行的操作是____________。
(4)实验室可用无水醋酸钠固体与碱石灰固体在加热的情况下制CH4,用此法来制取CH4,应选用的气体发生装置是__________(填字母,下同),可选用的气体收集装置是___________。
【题目】在食盐中加入适量的碘酸钾(KIO3),可预防碘缺乏病。
(1)人类膳食中缺碘易患_________
A 甲状腺肿大 B 贫血 C 骨质疏松症 D 软骨病
(2)某兴趣小组的同学,欲检测一袋食盐是否为加碘食盐,他们查阅资料得知,加碘食盐中的KIO3在酸性条件下能与KI溶液发生反应,生成碘(I2),淀粉遇I2变蓝色。现提供下列试剂和生活中常见的物质:
①KI溶液;②纯碱:③米汤;④白糖;⑤白酒:⑥白醋,该小组同学进行实验必须选用的试剂和物质是_______________
A ①③④ B ①③⑥ C ②④⑥ D ①④⑤
(3)该小组同学仔细阅读加碘食盐包装袋上的说明后,提出问题并与其他同学讨论,继续进行探究。
问题一:食盐是比较稳定的,而说明中强调“防热”,是否因为受热会造成碘的损失?
(实验一)探究温度对碘损失率的影响
老师指导他们将一定浓度的碘酸钾溶液分成5等份,在不同温度下加热十分钟后,用硫代硫酸
钠标准溶液测定碘酸钾溶液的浓度,计算碘损失率并记录如表:
温度 | 30℃水浴 | 50℃水浴 | 80℃水浴 | 100℃水浴 | 煮沸 |
碘损失率(%) | 0 | 0.3 | 0.67 | 1 | 5.56 |
①分析上表可得出的结论是_____________________________________
②人们常说:“炒菜时要后放碘盐,以免碘的损失。”这里的“碘”指的是____(填“碘单质”、“碘 元素”或“碘原子”)。
问题二:炒菜时加醋对碘的损失率是否也有影响?
(实验二)探究酸碱度对碘损失率的影响
③此组对照实验,要控制在加热的时间和温度、碘酸钾溶液的浓度和______均相同,溶液的酸碱度不同的条件下进行。
④实验需要调节溶液的酸碱性,下列物质不能选用的是_______(填字母)。
A 氢氧化钠 B 纯碱粉末 C 食盐晶体 D 稀盐酸
(4)碘酸钾中碘元素的质量分数为______。我国规定,食盐中加碘的含量为每千克食盐含腆0.035克,相当于每千克食盐含碘酸钾_____克。(精确到小数点后二位)