题目内容
【题目】某同学用锌和稀硫酸制取氢气.向气体发生装置中加入一定量锌粒,将15g稀硫酸分三次加入,每次生成气体的质量如下表。
次数 | 第一次 | 第二次 | 第三次 |
加入稀硫酸质量/g | 5 | 5 | 5 |
生成氢气质量/g | 0.02 | 0.02 | 0.01 |
请计算:
(1)共制得氢气_________g。
(2)所用稀硫酸的溶质质量分数为____________。
【答案】 0.05g 19.6%
【解析】(1)根据质量守恒定律,共制得氢气的质量是0.02g+0.02g+0.01g=0.05g。
(2)解∶设所用稀硫酸的溶质质量分数为x
Zn+H2SO4 =ZnSO4+H2↑
98 2
5g×x 0.02g
![]() =
=![]() ,x=19.6%。
,x=19.6%。
答∶(1)共制得氢气0.05g。(2)所用稀硫酸的溶质质量分数为19.6%。
点睛∶灵活运用质量守恒定律,正确书写化学方程式是顺利完成本题的重要前提。

 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案【题目】两百多年前,法国化学家拉瓦锡用定量的方法研究了空气成分。仿照这个实验的原理,化学家积极探索、不断创新,设计出下列如图所示的实验装置。
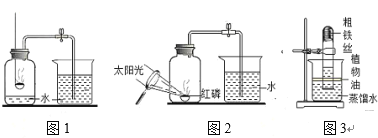
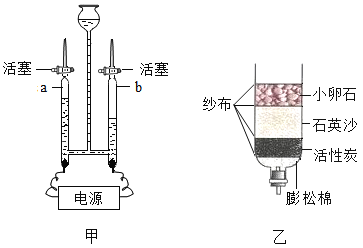
(实验回顾)图1是实验室用红磷燃烧来粗略测定空气中O2含量的装置。
(1)写出红磷燃烧的符号表达式__________。
(2)实验原理:由于红磷燃烧消耗空气中的O2,使容器内外产生__________,烧杯内的水倒吸入集气瓶中,通过量取进入水的体积可以粗略测得空气中O2的含量。
(3)实验结束,发现进入集气瓶中水的体积小于瓶内空气体积的1/5,可能原因是:①实验装置漏气;②__________;③…
(提出问题)测量结果与理论值误差较大,怎样才能减少误差呢?
(查阅资料)
①红磷着火点240℃,白磷着火点40℃;
②磷燃烧后的产物有毒;
③铁在潮湿的空气中会生锈,会消耗氧气。
(实验改进)
(1)甲组同学查阅资料后,对课本上的实验进行了图2所示的改进,其改进后的优点是__________(答一条)
(2)仪器改进后甲组同学测定的实验数据如下:
实验前 | 实验后 | ||
测定项目 | 集气瓶及止水夹左侧导管内空气的总体积 | 烧杯中水的体积 | 烧杯中剩余水的体积 |
体积/ | 126.0 | 80.0 | 54.8 |
根据上述实验可以算出,实验测得空气中O2的体积分数是__________%。
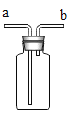
(3)乙组同学根据铁生锈原理,探究用铁能否测定空气中O2的含量,于是用粗铁丝进行了实验(装置如图3)。通过7天测得的数据计算出空气中O2的含量为20.13%。与红磷燃烧的方法相比,该方法的优点是铁丝生锈可以消耗更多的O2,使测量结果更准确,但也存在缺点,你认为缺点是__________。
(拓展延伸)铜也能与空气中氧气、水、二氧化碳反应,生成铜绿[铜绿的主要成分为Cu2(OH)2CO3]。若将图3装置中的粗铁丝换成足量的粗铜丝进行实验,请判断能否比较准确的测定空气中O2含量并说明理由_____________________。