题目内容
【题目】对分子、原子、离子的下列认识,其中正确的是
A.氢原子是最小的微粒,不可再分
B.镁原子的质子数大于镁离子的质子数
C.当液态水变成冰,水分子间不存在间隔
D.分子、原子、离子都可以直接构成物质
【答案】D
【解析】
试题分析:在化学变化中氢原子是最小的微粒,不可再分;原子变成离子时改变的是电子数,质子数不变;微观粒子间总是存在间隔的,当液态水变成冰,水分子间仍存在间隔;分子、原子、离子都可以直接构成物质,都可以保持物质的化学性质。

【题目】水是宝贵的自然资源,在工农业生产和日常生活中有着极其广泛的运用。
(一)水资源的现状:
(1) 我国淡水属于缺水国之列,人均淡水资源仅为世界人均量的1/4。北方,有些村庄打深井取用地下水。检验地下水是硬水还是软水,可以取水样加入少量 ,振荡,发现泡沫少,有较多浮渣产生,说明是硬水。使用硬水会给生产、生活带来麻烦,生活中常用 的方法来降低水的硬度。
(二)水的净化
(2)小刚收集到一瓶浑浊的河水,他要模拟自来水厂的净水过程,最终制成蒸馏水。其实验过程如下图所示。则:图中A物质是一种絮凝剂,它的名称是 ;操作①的名是 ;操作②主要是除去水中的一些异味和色素,应选用的物质是

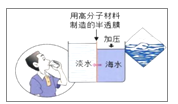
(3)海水淡化主要是为了提供饮用水和农业用水,目前淡化膜法是市场中的主流。高分子半透膜只允许水透过,盐类物质不能透过。海水淡化过程属于 变化。(填“物理”或“化学”)。
(三)水资源的利用
(4)水在生产生活中常用于溶解物质形成溶液。实验室溶解物质时,用到的玻璃仪器有烧杯和
(5)水一种重要的营养物质,被称为“六大营养素”之首。 病人输液时常用生理盐水【0.9%的氯化钠溶液】。医用生理盐水是 (选填“纯净物”“混合物”)。
(6)分解水可以得到氢气。氢气是一种可燃性气体。由于其清洁、高效、安全、可贮存、可运输等诸多优点,被称为“最理想的绿色能源”。
如图是电解水的简单装置:根据图中现象判断,乙试管内的气体可以用 来检验;实验证明水是由 组成的;
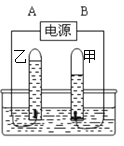
电解水要消耗大量的电能,科学家正致力于用其他方法由水制氢气,如用TiO2作催化剂,经光照可分解水得到氢气,该反应用化学式表示为 。
(7)下表是兴趣小组同学一次电解水实验测得的实际数据:
电解时间 | 1 | 2 | 3 | 4 | 5 | 6 | … |
负极生成气体体积/mL | 6 | 12 | 20 | 29 | 39 | 49 | … |
正极生成气体体积/mL | 2 | 4 | 7 | 11 | 16 | 21 | … |
分析表中的数据你发现的问题是 ,产生这一问题的原因可能是 。
(8)【已知通常状况下气体的密度:H2 : 0.089g/L O2: 1.429 g/L】。试根据电解水正、负两极所得气体体积的理论值,计算正、负两极所得气体的质量比为 ︰ (结果取整数)
【题目】下列为实验室常用的实验装置,回答问题
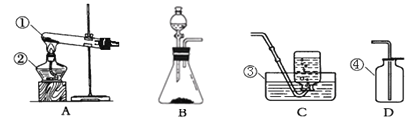
(1)请写出有标号仪器的名称:② ;③ 。
(2)实验室用高锰酸钾制氧气应选用的发生装置是 (填序号),装入药品前应先 ;如用C装置收集O2,则气体收集完毕时,应先__ ,如果用上述装置收集到的氧气不纯,可能的原因是 ,高锰酸钾制氧气反应的文字表达式是 。
(3)实验室制CO2反应文字表达式为 ;此外,也可用加热碳酸氢钠(NaHCO3)固体(产物为碳酸钠、二氧化碳、水)来制取CO2,该反应应选用的发生装置为 ,收集宜用装置 。实验室不可用加热碳酸氢铵固体来制取CO2的原因是 。
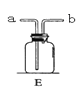
(4)若用右图E装置收集氧气应从 处进气(填“a”或“b”);检验已收满的方法是 ,若在E中装满水用排水法来收集氧气应从 处进气。
(5)用B制取氧气比A制取氧气的优点是 (填编号)。
A.生成物只有氧气 B.反应不需加热节能
C.便于控制反应速率 D.生成物对环境没有污染
(6)某科学兴趣小组学习二氧化锰(MnO2)催化分解过氧化氢的实验后,进行如下实验:a. 选择装置并检查气密性。b.称取0.1克的二氧化锰(MnO2)粉末加入容器中。c.量取50毫升溶质质量分数约5%的过氧化氢溶液加入容器中,记录一定时间内收集到的气体体积。改变二氧化锰的质量,重复上述实验,记录数据如下。(溶解到水中的氧气忽略不计)
时间/秒 | 生成氧气的体积/毫升 | |||
0.1克MnO2 | 0.2克MnO2 | 0.3克MnO2 | 0.4克MnO2 | |
40 | 49 | 61 | 75 | 86 |
80 | 77 | 87 | 90 | 92 |
120 | 89 | 92 | 92 | 92 |
160 | 92 | 92 | 92 | 92 |
①写出过氧化氢溶液与二氧化锰混合物制取氧气反应的文字或符号表达式 。
②该学习小组利用上述发生装置中的 (填“A”或“B”)与下列装置中的 (填编号)连接测量O2的体积。
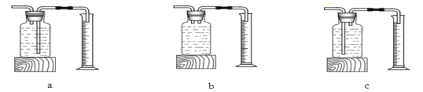
③实验结论:在相同条件下, ,双氧水分解得越快。
④实验反思:由上述实验测得的氧气体积总是偏大的可能原因是 。