题目内容
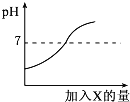
【题目】向稀盐酸中逐渐加入试剂X后,溶液的pH变化如图所示。试剂X是下列物质中的( )
A. NaOH B. H2O C. Mg D. CaCO3
【答案】A
【解析】
A、氢氧化钠显碱性,氢氧化钠和稀盐酸发生中和反应,溶液的酸性减弱,当恰好完全反应时溶液的pH值为7,继续加入氢氧化钠则溶液呈碱性,而使pH值大于7,图像与之相符,故A 正确;
B、加水可以稀释稀盐酸,溶液的酸性变弱,溶液的pH值增大,溶液始终呈酸性,溶液的pH值不会大于7,图像与之不相符,故B 错误;
C、镁为活泼金属,能与稀盐酸反应生成氯化镁和氢气,稀盐酸被消耗,溶液的pH值增大,但是溶液的pH值不会大于7,图像与之不相符,故C 错误;
D、碳酸钙能与稀盐酸反应,稀盐酸被消耗,溶液的pH值增大,但是溶液的pH值不会大于7,图像与之不相符,故D 错误。故选A。

练习册系列答案
相关题目
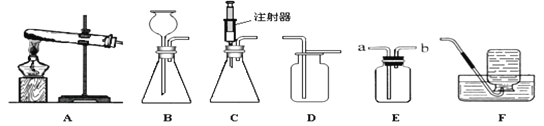
【题目】资料显示,不同年份生产的5角人民币硬币成分为:长城系列(1980—1986),铜锌合金;梅花系列(1991—2001),铜锌合金;荷花系列(2002—2007),钢芯镀铜。锌铜合金因是金黄色的俗称黄铜。为测定一种锌铜合金中锌的含量,取该合金放入如图盛有稀硫酸的锥形瓶中(注:充分反应后稀硫酸有剩余),多次实验后,取平均值所得数据如下表:
反应前 | 充分反应后装置及反应剩余物质质量 | |
装置和足量的稀硫酸质量 | 锌铜合金质量 | |
342.1g | 16g | 357.7g |
请计算:


(1)生成氢气的质量_______。
(2)该合金中锌的质量分数_________。