题目内容
【题目】胆矾(CuSO45H2O)在工农业生产中有广泛的用途。实验室利用废旧电池的铜帽(主要含铜和锌)为原料制备胆矾。实验流程如图所示:
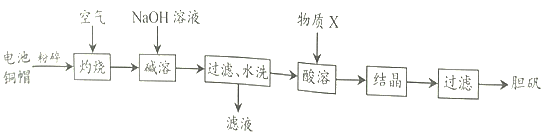
查阅资料:氧化锌能溶于氢氧化钠溶液。
(1)废旧电池铜帽的表面常有油污,可用洗洁精预先除去,洗洁精在除去油污的过程中起______作用。
(2)“碱溶”步骤中,为加快反应速率可采取多种措施,如搅拌、______等。
(3)“酸溶”时,发生反应的化学方程式是______。
(4)“灼烧”完全(已充分反应)的判断依据是______。
【答案】乳化 加热或增大氢氧化钠溶液的浓度 CuO+ H2SO4 =CuSO4+H2O 固体质量不再增加
【解析】
(1)根据洗洁精在除去油污的过程中起乳化作用进行分析;
(2)根据增大反应速率的因素进行分析;
(3)根据氧化铜和硫酸反应生成硫酸铜和水进行分析;
(4)根据铜和氧气加热生成氧化铜,锌和氧气加热生成氧化锌进行分析。
(1)洗洁精在除去油污的过程中起乳化作用;
(2))“碱溶”步骤中,为加快反应速率可采取多种措施,如搅拌、加热或增大氢氧化钠溶液的浓度等;
(3)氧化铜和硫酸反应生成硫酸铜和水,化学方程式为:CuO+ H2SO4 =CuSO4+H2O;
(4)铜和氧气加热生成氧化铜,锌和氧气加热生成氧化锌,所以“灼烧”完全(已充分反应)的判断依据是:固体质量不再增加。

【题目】农业上常用饱和食盐水进行选种.小明家现有某浓度的氯化钠溶液50kg,为了确定该氯化钠溶液的浓度,小明取出70克该溶液进行实验,得到下列数据
蒸发水的质量/g | 10 | 20 | 30 | 40 | 50 |
冷却到室温时析出氯化钠的质量/g | 0 | 0 | 0 | 2.8 | 6.4 |
(1)原溶液中氯化钠的质量分数;
(2)在50kg氯化钠溶液中加入多少千克氯化钠刚好成为该室温时的饱和溶液?