题目内容
构建知识网络,可以帮助我们理解知识间的内在联系,如图是关于铁化学性质的知识网络.请回答下列问题: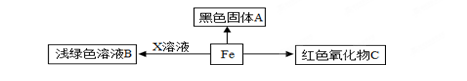
(1)铁丝在氧气中燃烧生成黑色固体A,写出A的化学式
(2)写出防止铁生锈的一种方法
(3)若要证明Fe、Cu、Ag三种金属的活动性顺序,只需选用Fe、Ag和X溶液三种试剂,X是 溶液,写出发生反应的化学方程式 ,该反应的基本类型是 .
(4)若X为稀硫酸,向Fe和X溶液反应后的溶液中加入一定量的锌粉,有气泡产生,充分反应后过滤,得到滤渣和滤液,下列对滤渣和滤液中溶质的成分分析正确的是
| A.滤液中一定含有FeSO4和ZnSO4 | B.滤渣中只含有Fe |
| C.滤液中一定含有ZnSO4 | D.滤渣中一定含有Zn和Fe. |
(1)Fe3O4
(2)涂油(刷漆)
(3)硫酸铜 Fe+CuSO4= Cu+FeSO4 置换反应
(4) C
解析试题分析:(1)金属铁的化学性质:铁丝在氧气中燃烧生成黑色固体四氧化三铁,化学式:Fe3O4
(2)铁生锈的条件:与氧气、水接触,所以防止铁生锈的原理就是隔绝氧气和水,具体的措施;1、保持铁制品表面的清洁、干燥,2、表面涂保护膜:如涂油、刷漆、电镀、烤蓝等,3、改变铁的单一结构,制成不锈钢等
(3)要证明Fe、Cu、Ag三种金属的活动性顺序,可利用两个原理:1、利用金属与酸反应,2、利用金属与盐溶液反应,根据题目所选Fe、Ag和X溶液三种试剂,利用的是金属与盐溶液,所以x是硫酸铜溶液,分别将Fe、Ag加入到硫酸铜溶液中,铁会反应,银不反应,所以发生的化学方程式为: Fe+CuSO4= Cu+FeSO4,反应的基本类型是置换反应
(4)若X为稀硫酸,发生的反应是:Fe + H2SO4 = FeSO4 + H2↑,此时反应后溶液中的溶质有两种可能性:1、只有FeSO4,2、H2SO4和FeSO4混合溶液,因为向Fe和X溶液反应后的溶液中加入一定量的锌粉,有气泡产生,说明是第二种情况,然后根据“弱者先出局”的原则,加入的锌粉是先与H2SO4和FeSO4混合溶液中的H2SO4反应,若有剩余继续与FeSO4反应,因为有滤渣,说明锌一定与FeSO4发生了反应,把铁置换出来了,但到底是全部置换还是部分置换,那就取决于锌的量,当然若锌的量足够,那就能把铁全部置换,这样滤液中就只有ZnSO4,滤渣中含有Zn和Fe,若锌的量不够,把铁部分置换,这样滤液中就有FeSO4和ZnSO4,滤渣中就只含有Fe,所以选C正确
考点:金属铁的化学性质,金属的活动性顺序

 教材全解字词句篇系列答案
教材全解字词句篇系列答案 (8分)2014年央视 “3.15”晚会上曝出某品牌金饰品掺假的事件,引起同学们的好奇。小明同学拿来一片黄色的金属,和小军同学一起进行了相关探究活动。
【猜 想】①小明认为是黄金 ②小军认为是铜锌合金
【设计实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 取一小片黄色金属放在石棉网上用酒精灯加热 | 黄色的金属变黑 |
| ② | 取一小片黄色的金属放入稀硫酸中 | |
(1)由实验①可知,猜想 (填序号)正确;写出反应的化学方程式
。
(2)实验②中的现象是 ,写出反应的化学方程式
。
【反思应用】假设你的观点和小军相同,请你选用一种类别不同于稀硫酸的试剂,再设计一个实验:取一小片黄色的金属放入 溶液中,实验中观察到的现象是 。
(6分)请按下列要求选择合适的物质,用其相应的字母填空。
| A.甲烷 | B.干冰 | C.硝酸钾 | D.不锈钢 E.小苏打 F.聚乙烯塑料 |
(3)用于人工降雨的是____ (4)治疗胃酸过多___,
(5)用作复合肥是____ (6)天然气的主要成分____
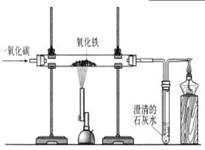



 H2SO4请写出该反应的化学方程式: .
H2SO4请写出该反应的化学方程式: .