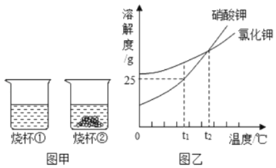
题目内容
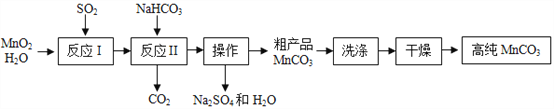
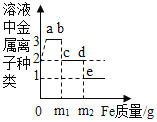
【题目】MgSO47H2O是一种重要的化工原料,某工厂以一种镁矿石(主要成分为SiO2和MgCO3,还含有少量FeCO3)为原料制备MgSO47H2O的主要流程如图1:
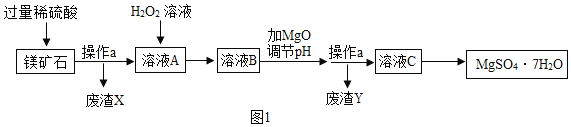
已知:SiO2既不溶于水也不溶于稀硫酸。请回答下列问题
(1)“操作a”的名称是_____,“废渣Y”中含有少量的 FeOOH,其中铁元素的化合价是_____。
(2)MgCO3溶于稀硫酸的化学方程式为_____“溶液A”中加入H2O2溶液会生成Fe2(SO4)3,该反应的化学方程式为_____。
(3)选用MgO调节pH而不选用NaOH的原因是_____。
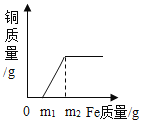
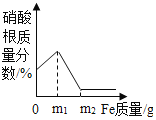
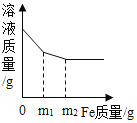
(4)向盛有100g C溶液的烧杯中加入40g氢氧化钠溶液至恰好完全反应(如图2),过滤,称量滤液质量为134.2g,求
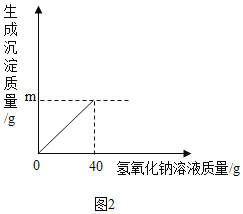
①图象中m的值为_____。
②所加氢氧化钠溶液中溶质的质量分数是______。(写出必要的计算过程)
【答案】过滤 +3 MgCO3+H2SO4=MgSO4+H2O+CO2↑ 2FeSO4+H2SO4+H2O2=Fe2(SO4)3+2H2O 氢氧化钠和硫酸反应会生成新的杂质硫酸钠 5.8 20%
【解析】
(1)操作a是把不溶性固体和液体相分开的操作,是过滤,化合物中各元素化合价代的数和为零,氧为﹣2价,氢为+1价,所以“废渣Y”中含有少量的 FeOOH,其中铁元素的化合价是+3;
(2)碳酸镁和稀硫酸反应生成硫酸镁、水和二氧化碳,化学方程式为:![]()
![]() ;溶液A中含有硫酸亚铁和硫酸,加入过氧化氢,发生化学反应生成硫酸铁和水,化学方程式为:
;溶液A中含有硫酸亚铁和硫酸,加入过氧化氢,发生化学反应生成硫酸铁和水,化学方程式为:![]() ;
;
(3)除杂的原则:除去杂质,不能引入新的杂质,所以选用MgO调节pH使Fe3+转化为沉淀,而不选用NaOH的原因是:氢氧化钠和硫酸反应会生成新的杂质硫酸钠;
(4)①根据质量守恒定律,生成的氢氧化镁的质量为:
100g+40g﹣134.2g=5.8g;
②设生成5.8g沉淀需要氢氧化钠的质量为x。

![]() x=8g
x=8g
所加氢氧化钠溶液中溶质的质量分数为:
![]() =20%
=20%
答:所加氢氧化钠溶液中溶质的质量分数为20%。

 名校课堂系列答案
名校课堂系列答案【题目】阅读下面短文,回答相关问题。
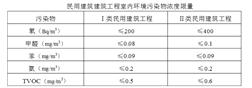
甲醛(HCHO),无色气体,有特殊的刺激气味,对人眼、鼻等有刺激作用。它是装修中不可避免的装修污染,它广泛存在于板材的粘合剂和其他的家具中,然后不断地挥发,给家居空间造成不同程度的污染。甲醛是原浆毒物,能与蛋白质中的胺基-NH2结合,使蛋白质性质发生改变,或称变性。当甲醛浓度在空气中达到0.06-0.07mg/m3时,儿童就会发生轻微气喘;达到0.1mg/ m3时,就有异味和不适感;达到0.5mg/ m3时,可刺激眼睛,引起流泪;达到0.6mg/ m3,可引起咽喉不适或疼痛。浓度更高时,可引起恶心呕吐,咳嗽胸闷,气喘甚至肺水肿;达到30mg/ m3时,会立即致人死亡,因此,我国早已制定并执行着民用建筑环境污染物限量的标准(见表1)。
为减少甲醛等有害物质的伤害,首先,要从控制污染源做起,减少接触甲醛的机会,由于甲醛释放时间非常久,最长能够达到15年,把控好建材和家具的品质至关重要。
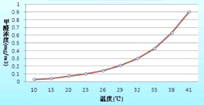
其次,释放甲醛。最有效的方法就是开窗通风,表2所示,甲醛的挥发受温度影响很大,因此,正确的做法是把门窗先关后开,关窗有利于升温,几天后再开窗会更好的让甲醛的气味消散出去。
|
|
表1 | 表2 |
第三,吸收甲醛。利用绿萝、吊兰、常春藤等植物吸收;利用活性炭其内部发达的孔隙结构能够捕捉甲醛分子,降低室内空气中的甲醛浓度;利用央视推荐的紫加黑除甲醛,其氧化分解原理对甲醛较为有效,能够把甲醛分解为二氧化碳和水。
甲醛超标对家人的危害很大,装修新房时尽量简装修降低复合板材的使用度,根据甲醛的基本性质和合理除甲醛方法治理甲醛,只有室内甲醛低于国家标准才能够入住。
(1)甲醛的相对分子质量为____。
(2)甲醛中毒的过程属于_____变化(填“物理”或“化学”)。
(3)甲醛对儿童、老人等影响最大,即使检测部门检测已达标的房间,儿童进入后也会发生轻微气喘,其原因是___。
(4)活性炭和紫加黑除甲醛的本质区别是____(从微观角度进行说明)。
(5)下列有关甲醛的说法正确的是____。
A 甲醛是无色、有特殊刺激气味的气体。
B 减少甲醛的危害,最重要的是要控制污染源,减少接触甲醛的机会。
C 每天开窗通风,并恒温在25℃,能够使甲醛很快释放完毕。
D 房间内栽培绿萝、吊兰等绿植,既美化环境,又可以吸收甲醛