题目内容
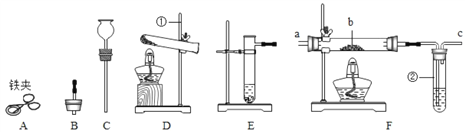
【题目】下图是一盏废旧台灯,某实验小组的同学利用它进行观察分析并完成相关实验。
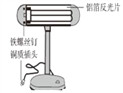
(1)小明发现台灯的铁螺丝钉表面已经锈蚀,原因是铁与空气中的_______等发生了化学反应。
(2)小红发现铝箔反光片呈银白色,无锈迹,原因是铝表面有一层致密的氧化膜,生成该氧化膜的化学方程式为_____________________________。
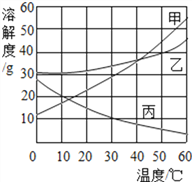
(3)铁、铝、铜的金属活动性由强到弱的顺序为____________。为了验证三者的金属活动性顺序,小志从实验室领来氯化铝溶液、硫酸铜溶液,并利用台灯提供的一种金属进行实验,即达到了实验目的。实验中发生反应的化学方程式为_________。实验结束后,发现滤液仍呈蓝色,则所得滤液中一定含有的阳离子是___________________________(填离子符号)。
【答案】 水蒸气和氧气 4Al + 3O2 = 2Al2O3 铝 > 铁 > 铜; Fe + CuSO4 = FeSO4 + Cu; Al3+、Fe2+、Cu2+
【解析】(1)铁在空气中锈蚀,实际上是铁跟空气中的氧气和水共同作用的结果;(2)常温下,铝在空气中与氧气反应生成氧化铝保护膜,写出反应的化学方程式即可;(3)由金属活动性顺序进行分析解答;验证金属的活动性顺序是否合理,可根据“反应则活泼,不反应则不活泼”进行分析判断;根据反应物是否过量分析解答。(1)台灯的铁螺丝钉表面已经锈蚀,原因是铁与空气中的氧气和水蒸气发生了化学反应;(2)常温下,铝在空气中与氧气反应生成氧化铝保护膜,反应的化学方程式为:4Al+3O2═2Al2O3;(3)由金属活动性顺序可知,铁、铝、铜的金属活动性由强到弱的顺序为铝 > 铁 > 铜(或Al>Fe>Cu);验证三者的金属活动性顺序,小志从实验室领来氯化铝溶液、硫酸铜溶液,可利用台灯提供的金属铁,铁能与硫酸铜溶液反应生成硫酸亚铁和铜,不能氯化铝溶液反应,可验证三者的金属活动性顺序;反应的化学方程式为Fe+CuSO4=FeSO4+Cu;实验结束后,发现滤液仍呈蓝色,说明硫酸铜溶液过量,则所得滤液中一定含有的阳离子是Al3+、Fe2+、Cu2+。

 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
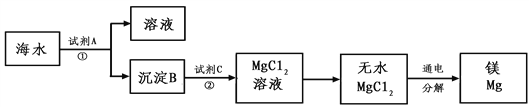
阳光课堂同步练习系列答案【题目】草酸镍晶体(NiC2O4·2H2O)可用于制镍催化剂。某小组用废镍催化剂(成分为Fe2O3、Ni、Fe、SiO2等)制备草酸镍晶体的部分实验流程如下:
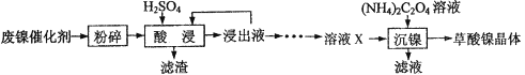
已知:①Ni能和稀H2SO4反应。
②相关金属离子生成氢氧化物沉淀的pH如下表:
金属离子 | 开始沉淀的pH | 完全沉淀的pH |
Fe3+ | 1.1 | 3.2 |
Fe2+ | 5.8 | 8.8 |
Ni2+ | 6.7 | 9.5 |
③H2O2能将Fe2+氧化为Fe3+
(1)废镍催化剂“粉碎”的目的是______。
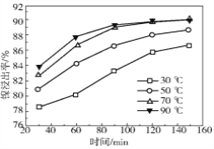
(2)保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率随时间变化如图,“酸浸”的适宜温度与时间分别为 _______(填字母)。
A.30℃、30min B.90℃、150min C.70℃、120min D.90℃、120min
(3)“酸浸”中发生的复分解反应方程式为________。
(4)“浸出液”得到“溶液x”过程中,加入试剂先后顺序是_____(填字母)。
A.先加H2O2溶液,再加NaOH溶液 B.先加NaOH溶液,再加H2O2溶液
加NaOH溶液调节pH_____(填范围),充分反应后得到滤渣的操作是______,该操作中所用到的玻璃仪器有玻璃棒、烧杯和_________。
(5)将“沉镍”工序:①主要过程为:蒸发浓缩、_____ 、过滤,所得固体用75%乙醇洗涤、110℃下烘干,得草酸镍晶体。
②用75%乙醇洗涤的目的是洗去杂质、___________;
③烘干温度不超过110℃的原因是______。