题目内容
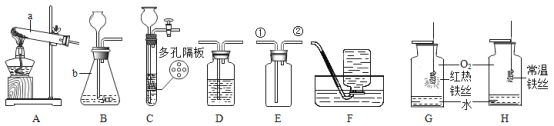
【题目】下图是实验室制取CO2及进行性质实验的部分装置。
(1) 大理石固体与稀盐酸反应生成CO2气体的化学方程式是______________。某实验中取用了100g大理石与足量的稀盐酸反应,得到4.4g二氧化碳气体,则该大理石中,碳酸钙的质量分数为_____________。
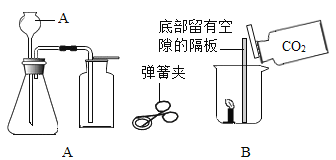
(2)检验装置气密性,按图连接装置,先用弹簧夹夹紧胶皮管,再加水至A的下端形成一段水柱,静置,若观察到_______,说明气密性良好。
(3)加入药品。添加块状大理石固体时,为避免打破锥形瓶,应将锥形瓶______________,再放入固体。添加盐酸时,将稀盐酸从_______(填仪器A的名称)倒入锥形瓶至_________。
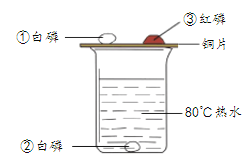
(4)如图所示,向放置有燃着的蜡烛的烧杯中倒入CO2,观察到的现象是_______________。由此可知二氧化碳的用途之一是__________________
(5)实验室常用稀硫酸和锌粒作为反应物来制取氢气,请你分析后判断,能否用上面A图中的整套装置来制取氢气?答:__________(填“能”或“不能”)。
【答案】CaCO3 + 2HCl = CaCl2 + H2O + CO2↑ 10% 水柱高度保持不变 倾斜 长颈漏斗 长颈漏斗下端管口被液体封住 蜡烛熄灭 灭火 不能
【解析】
(1)碳酸钙与稀盐酸反应生成氯化钙、二氧化碳和水,反应的方程式为:CaCO3 + 2HCl = CaCl2 + H2O + CO2↑。
设大理石中,碳酸钙的质量分数为x
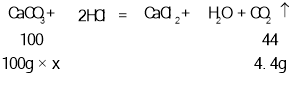
![]() ,解得x=10%
,解得x=10%
(2)该装置检查装置的气密性方法是按图连接装置,先用弹簧夹夹紧胶皮管,再加水至A的下端形成一段水柱,静置,若观察到水中不下降,气密性良好。
(3)向锥形瓶中添加碳酸钙时,为了防止打破锥形瓶,要将锥形瓶倾斜。稀盐酸有长颈漏斗加入锥形瓶,使长颈漏斗的下端形成液封为止。
(4)实验中观察到蜡烛熄灭,说明二氧化碳的密度比空气的密度大,不燃烧也不支持燃烧。
(5)氢气的密度比空气的密度小,难溶于水,故收集氢气应该用排水法或向下排空气法,故不能。

 一线名师提优试卷系列答案
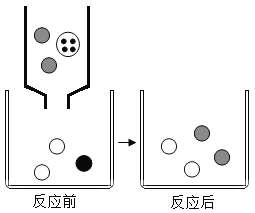
一线名师提优试卷系列答案【题目】在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如表所示,下列说法不正确的是( )
物质 | X | Y | Z | W |
反应前质量/g | 10 | 3 | 90 | 0 |
反应后质量/g | 3.2 | 3 | 待测 | 3.2 |
A. W可能是单质 B. Y可能是催化剂
C. 该反应是分解反应 D. 反应后Z物质的质量为![]()