题目内容
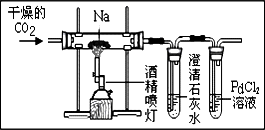
如图装置能生产一种高效、广谱、安全的次氯酸钠(NaClO)消毒液,其原理是氯化钠溶液在通电时发生如下反应:NaCl+H2O
NaClO+H2↑.
(1)若用该装置制取5000g质量分数为0.298%的次氯酸钠消毒液,请列式计算参加反应的氯化钠的质量.
(2)请说出使用该装置生产消毒液的一个优点和一个注意事项.
| ||
(1)若用该装置制取5000g质量分数为0.298%的次氯酸钠消毒液,请列式计算参加反应的氯化钠的质量.
(2)请说出使用该装置生产消毒液的一个优点和一个注意事项.

(1)根据题意可以知道要制取的次氯酸钠的质量为:5000g×0.298%=14.9g
设参加反应的氯化钠的质量为X
NaCl+H2O
NaClO+H2↑
58.5 74.5
X 14.9g
=
解得:X=11.7g
答:参加反应的氯化钠的质量为11.7g;
(2)根据所发生的反应可以知道,在通电的条件下用氯化钠来制取次氯酸钠,原料比较简单,操作也很方便,但是在反应过程中产生了氢气,而氢气可以燃烧,所以要及时的处理氢气,以免发生危险.
故答案为:(1)11.7g;
(2)方便、快捷;生成的可燃性气体,要及时处理,以免出现危险.
设参加反应的氯化钠的质量为X
NaCl+H2O
| ||
58.5 74.5
X 14.9g
| 58.5 |
| 74.5 |
| X |
| 14.9g |
解得:X=11.7g
答:参加反应的氯化钠的质量为11.7g;
(2)根据所发生的反应可以知道,在通电的条件下用氯化钠来制取次氯酸钠,原料比较简单,操作也很方便,但是在反应过程中产生了氢气,而氢气可以燃烧,所以要及时的处理氢气,以免发生危险.
故答案为:(1)11.7g;
(2)方便、快捷;生成的可燃性气体,要及时处理,以免出现危险.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
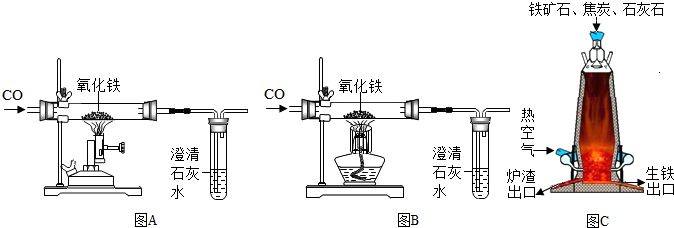

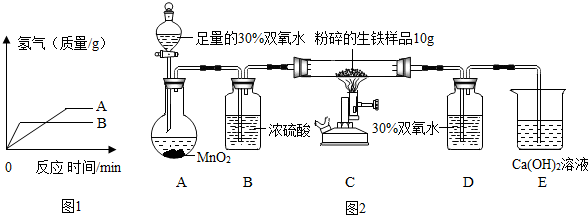
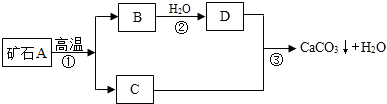
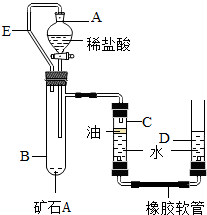 【实验原理】:测定一定质量的矿石A与足量稀盐酸反应产生的二氧化碳在常温常压下的体积,根据密度求出二氧化碳的质量,然后根据发生的化学反应方程式算出矿石A中碳酸钙的质量,进而求出矿石A中碳酸钙的质量分数.
【实验原理】:测定一定质量的矿石A与足量稀盐酸反应产生的二氧化碳在常温常压下的体积,根据密度求出二氧化碳的质量,然后根据发生的化学反应方程式算出矿石A中碳酸钙的质量,进而求出矿石A中碳酸钙的质量分数.