题目内容
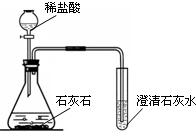 某化学兴趣小组用下图装置制取并检验二氧化碳.实验过程中,可观察到试管里产生
某化学兴趣小组用下图装置制取并检验二氧化碳.实验过程中,可观察到试管里产生【提出问题】沉淀为什么能溶解变成澄清溶液?
【查阅资料】碳酸盐溶于酸;碳酸氢钙[Ca(HCO3)2]溶于水.
【猜想与假设】①溶液呈酸性;②反应生成了碳酸氢钙.
【实验与结论】
| 实验操作 | 实验现象 | 实验结论 |
| 实验Ⅰ:把一小片pH试纸放在一块干净的玻璃片上,用 |
测得被测液的pH=8 | 猜想① (填“成立”或“不成立”) |
| 实验Ⅱ:取沉淀溶解成的澄清溶液于另一支试管中,加入 |
有气泡产生 | 反应的化学方程式为: 猜想②成立. |
考点:二氧化碳的实验室制法,溶液的酸碱度测定,二氧化碳的检验和验满,溶液的酸碱性与pH值的关系,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳;二氧化碳和氢氧化钙反应生成碳酸钙白色沉淀和水.实验与结论:把一小片pH试纸放在一块干净的玻璃片上,用玻璃棒蘸取A溶液沾在试纸上,把试纸呈现的颜色与标准比色卡对照,测得被测液的pH=8,说明溶液呈碱性,因此猜想①不成立;取A溶液于另一支试管中,加入稀盐酸,有气体产生,猜想②成立;碳酸氢钙和盐酸反应生成氯化钙钙和水和二氧化碳,配平即可.从探究中得到的启示是:不溶物在一定条件下可转化为可溶物,或条件不同,产物不同等.
解答:解:二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,即生成白色沉淀,就证明是二氧化碳;二氧化碳和氢氧化钙反应生成碳酸钙白色沉淀和水,故答案为:白; CO2+Ca(OH)2=CaCO3↓+H2O;
实验Ⅰ:把一小片pH试纸放在一块干净的玻璃片上,用玻璃棒蘸取溶液沾在试纸上,把试纸呈现的颜色与标准比色卡对照,测得被测液的pH=8,说明溶液呈碱性,因此猜想①不成立,故答案为:玻璃棒; 不成立;
实验Ⅱ:取溶液于另一支试管中,加入稀盐酸,有气体产生,猜想②成立;碳酸氢钙和盐酸反应生成氯化钙钙和水和二氧化碳,配平即可,故答案为:稀盐酸;2HCl+Ca(HCO3)2=CaCl2+2H2O+2CO2↑;
根据题意,碳酸钙与二氧化碳、水发生化合反应生成可溶于水的碳酸氢钙,方程式是CaCO3+H2O+CO2=Ca(HCO3)2;故答案为:CaCO3+H2O+CO2=Ca(HCO3)2.
实验Ⅰ:把一小片pH试纸放在一块干净的玻璃片上,用玻璃棒蘸取溶液沾在试纸上,把试纸呈现的颜色与标准比色卡对照,测得被测液的pH=8,说明溶液呈碱性,因此猜想①不成立,故答案为:玻璃棒; 不成立;
实验Ⅱ:取溶液于另一支试管中,加入稀盐酸,有气体产生,猜想②成立;碳酸氢钙和盐酸反应生成氯化钙钙和水和二氧化碳,配平即可,故答案为:稀盐酸;2HCl+Ca(HCO3)2=CaCl2+2H2O+2CO2↑;
根据题意,碳酸钙与二氧化碳、水发生化合反应生成可溶于水的碳酸氢钙,方程式是CaCO3+H2O+CO2=Ca(HCO3)2;故答案为:CaCO3+H2O+CO2=Ca(HCO3)2.
点评:本考点主要考查了二氧化碳的检验,同时也考查了化学方程式的书写和PH的测定等,综合性比较强.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
葡萄糖在人体组织中缓慢氧化放出热量,这是人类生命活动所需要的重要来源之一.葡萄糖的化学式为C6H12O6,从这个化学式中得到的信息中错误的是( )
| A、葡萄糖由碳、氢、氧三种元素组成 |
| B、一个葡萄糖分子中共有24个原子 |
| C、葡萄糖是由碳、氢、氧三种原子构成 |
| D、碳、氢、氧三种元素质量比为6:12:6 |

 指出如图倾倒药剂时错误之处:
指出如图倾倒药剂时错误之处: