题目内容
 (2013?松江区三模)在化学实验室,小明发现一瓶没有密封好的NaOH已经结块.
(2013?松江区三模)在化学实验室,小明发现一瓶没有密封好的NaOH已经结块.[提出问题]结块后的固体成分是什么?
[猜想与假设]
用化学方程式表示氢氧化钠在空气中发生的反应:
CO2+2NaOH═Na2CO3+H2O
CO2+2NaOH═Na2CO3+H2O
.猜想一:固体为碳酸钠.
猜想二:固体为
氢氧化钠和碳酸钠
氢氧化钠和碳酸钠
.[查阅资料]Na2CO3溶液pH>7,BaCl2溶液pH=7,
Ca(NO3)2溶液pH=7,CaCl2溶液pH=7,
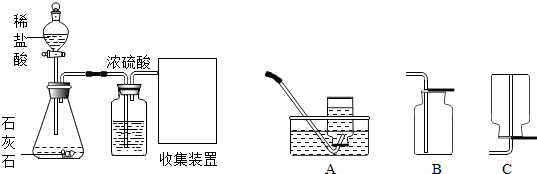
[进行实验]从瓶中取出一定量的固体,加入足量水溶解,再将溶液分三等份分别加入A、B、C三种试剂,进行如下实验.
[实验分析]根据实验现象,可判断出结块固体中一定有碳酸钠,请写出不同类别的三种试剂:A
盐酸
盐酸
.B氢氧化钙溶液
氢氧化钙溶液
.C氯化钙溶液
氯化钙溶液
.[实验设计]为进一步确定固体的成分,小明从实验室里选了两种试剂,先向样品中加入过量的
氯化钙
氯化钙
溶液,然后过滤,再向滤液中加入酚酞试液
酚酞试液
,现象是溶液变红
溶液变红
,于是判断出结块固体中一定还有氢氧化钠.分析:根据已有的知识进行分析,氢氧化钠容易与二氧化碳反应生成碳酸钠而变质,碳酸钠溶液遇酸化气,能与含有可溶性钙离子的物质反应生成碳酸钙沉淀,据此解答即可.
解答:解:(猜想与假设)氢氧化钠容易和二氧化碳发生反应而生成了碳酸钠和水,故填:CO2+2NaOH═Na2CO3+H2O;
猜想二:氢氧化钠可能部分变质,故固体中含有氢氧化钠和碳酸钠,故填:氢氧化钠和碳酸钠;
实验分析:实验证明,一定含有碳酸钠,依据碳酸钠的性质,碳酸钠能与盐酸反应生成二氧化碳气体,能与氢氧化钙溶液反应生成碳酸钙沉淀,能与氯化钙溶液反应生成碳酸钙沉淀,故选用的试剂可以是盐酸、氢氧化钙和氯化钙,故填:盐酸,氢氧化钙溶液,氯化钙溶液;
实验设计:要证明含有氢氧化钠,需要排除碳酸钠对氢氧化钠的干扰,可以加入氯化钙溶液使碳酸钠转化生成碳酸钙沉淀,然后加入酚酞试液,如果酚酞变红,说明含有氢氧化钠,故填:氯化钙,酚酞试液,溶液变红.
猜想二:氢氧化钠可能部分变质,故固体中含有氢氧化钠和碳酸钠,故填:氢氧化钠和碳酸钠;
实验分析:实验证明,一定含有碳酸钠,依据碳酸钠的性质,碳酸钠能与盐酸反应生成二氧化碳气体,能与氢氧化钙溶液反应生成碳酸钙沉淀,能与氯化钙溶液反应生成碳酸钙沉淀,故选用的试剂可以是盐酸、氢氧化钙和氯化钙,故填:盐酸,氢氧化钙溶液,氯化钙溶液;
实验设计:要证明含有氢氧化钠,需要排除碳酸钠对氢氧化钠的干扰,可以加入氯化钙溶液使碳酸钠转化生成碳酸钙沉淀,然后加入酚酞试液,如果酚酞变红,说明含有氢氧化钠,故填:氯化钙,酚酞试液,溶液变红.
点评:本题考查了变质物质成分的推断,完成此题,可以依据物质的性质进行,书写反应的化学方程式要注意配平.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
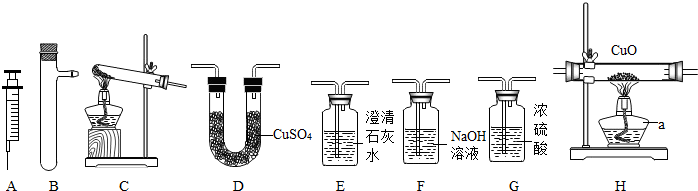 a
a