题目内容
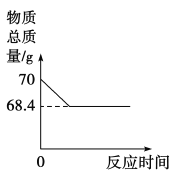
【题目】同学们用碳酸钠溶液和浓盐酸来研究简易灭火器的反应原理时,对废液的成分进行了探究.
(推理假设)上述两种物质反应的化学方程式为 ______________________ .由此推测出反应后废液中的溶质一定有_______,可能有碳酸钠或盐酸.
(实验探究)
(一)确定废液中是否含有盐酸
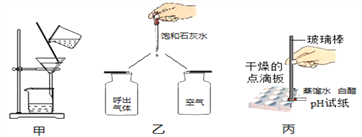
(1)选择试剂:根据盐酸的化学性质,同学们选用了如图所示的五种物质,其中物质X是酸碱指示剂中的 ______ 溶液.
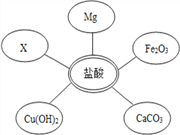
(2)实验验证:某同学甲向废液中加入少量的镁粉,观察到 __________ ,确定废液中一定没有盐酸.
(二)确定废液中是否含有碳酸钠
某同学选用 ______ 测出废液的pH=10,由此确定废液中_______________。
(三)处理废液,回收利用
欲从废液中得到纯净的NaCl,设计了如下实验方案,请完成方案评价.
方案 | 加入试剂 | 分离方法 | 方案评价 |
一 | 适量的Ca(NO3)2溶液 | 过滤、蒸发结晶 | ______ (选填“可行”或“不可行”,下同) |
二 | 适量的稀盐酸 | 蒸发结晶 | ______ |
【答案】 Na2CO3+2HCl=2NaCl+H2O+CO2↑ 氯化钠 紫色石蕊 无明显现象(或没有气泡) pH试纸 一定含有碳酸钠 不可行 可行
【解析】【推理假设】两种物质反应的化学方程式为Na2CO3+2HCl=2NaCl+H2O+CO2↑。推测出反应后废液中的溶质一定有氯化钠,可能有碳酸钠或盐酸。【实验探究】(一)确定废液中是否含有盐酸。(1) 根据盐酸的化学性质,物质X是酸碱指示剂中的紫色石蕊溶液,遇酸变红,遇碱变蓝。(2) 向废液中加入少量的镁粉,观察到无明显现象(或没有气泡),镁与盐酸反应产生气体氢气,确定废液中一定没有盐酸。(二)确定废液中是否含有碳酸钠。选用pH试纸测出废液的pH=10,由此确定废液中一定含有碳酸钠,碳酸钠溶液呈碱性,pH>7溶液呈碱性。(三)处理废液,回收利用,从废液中得到纯净的NaCl。
方案 | 加入试剂 | 分离方法 | 方案评价 |
一 | 适量的Ca(NO3)2溶液 | 过滤、蒸发结晶 | 不可行,Ca(NO3)2 与碳酸钠反应生成碳酸钙白色沉淀和硝酸钠。 |
二 | 适量的稀盐酸 | 蒸发结晶 | 可行,稀盐酸与碳酸钠反应生成氯化钠,水和二氧化碳。 |
点睛∶碳酸钠溶液和浓盐酸反应生成氯化钠,水和二氧化碳。紫色石蕊溶液,遇酸变红,遇碱变蓝。除杂原则⑴杂质尽量除净,⑵在除去一种杂质的同时不应增添新的杂质,⑶在除去杂质的同时,非杂物质不应过多消耗,但质量可以增加。