题目内容
【题目】袋装食品中常用一种“双吸剂”保持,主要成分是铁粉和生石灰,同学们对一久置的双吸剂固体样品很好奇,设计了如下实验进行探究.
【提出问题】久置“双吸剂”的成分是什么?
【做出猜想】久置“双吸剂”中可能有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3
【实验探究1】取固体样品研磨,用磁铁吸引,磁铁上沾有黑色粉末,说明“双吸剂”中一定有_______.再用磁铁反复吸引后,残留固体用于后续探究活动.
【实验探究2】
实验操作 | 实验现象 | 实验结论 |
取少量探究实验1的残留固体放入试管中,加入蒸馏水。 | 试管外壁不发烫 | 固体中一定没有 _____________ |
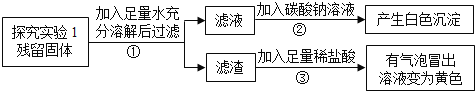
【实验探究3】
【实验结论】
(1)步骤②产生白色沉淀,说明久置的“双吸剂”中含有_________,其反应的化学方程式:___________________。
(2)步骤③有气泡冒出,溶液变为黄色,说明久置的“双吸剂”中含有_______和______。所涉及的两个反应的化学方程式为:_______________;_____________________。
【答案】 Fe CaO Ca(OH)2 Ca(OH)2 + Na2CO3 ====2NaOH + CaCO3↓ CaCO3 Fe2O3 CaCO3 + 2HCl===CaCl2+H2O+CO2↑ Fe2O3+6HCl===2FeCl3+3H2O
【解析】【实验探究1】铁能被磁铁吸引且颜色是黑色的,所以用磁铁吸引,磁铁上沾有黑色粉末,说明“双吸剂”中一定有Fe;
【实验探究2】氧化钙和水反应生成氢氧化钙要放出大量的热,所以取少量探究实验1的残留固体放入试管中,加入蒸馏水,试管外壁不发烫,说明固体中一定没有CaO;
【实验结论】(1)碳酸钠溶液能和氢氧化钙溶液反应生成碳酸钙白色沉淀和氢氧化钠,所以步骤②产生白色沉淀,说明久置的“双吸剂”中含有氢氧化钙,反应的化学方程式:Ca(OH)2+ Na2CO3 = 2NaOH + CaCO3↓;
(2)盐酸和碳酸钙反应生成二氧化碳气体,盐酸能和氧化铁反应生成氯化铁和水,氯化铁溶液的颜色是黄色的,所以步骤③有气泡冒出,溶液变为黄色,说明久置的“双吸剂”中含Fe2O3、CaCO3;化学方程式为:CaCO3 + 2HCl=CaCl2+H2O+CO2↑;Fe2O3+6HCl=2FeCl3+3H2O。

【题目】下表列出了除去物质中所含少量杂质的方法,其中不正确的选项是( )
选项 | 物质 | 所含杂质 | 除去杂质的方法 |
A | FeCl2溶液 | CuCl2溶液 | 加入过量的铁粉,过滤 |
B | CaCO3粉末 | NaCl粉末 | 加水溶解、过滤、洗涤、烘干 |
C | 氯化钾 | 氯酸钾 | 加热 |
D | 氢氧化钠溶液 | 氢氧化钙溶液 | 通入CO2,过滤 |
A. A B. B C. C D. D