题目内容
28、实验室用含有少量碳酸镁杂质的块状碳酸钙与盐酸反应制取二氧化碳.
(1)通过长颈漏斗向放有块状碳酸钙的大试管中加入足量的盐酸,充分反应,在大试管中可以观察到的现象是
(2)反应完毕,欲从反应液中制取少量纯净的氯化钙晶体,拟进行下列几项操作:
①蒸发 ②过滤 ③加入适量的X溶液
X的化学式是
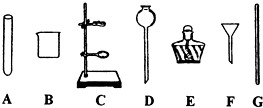
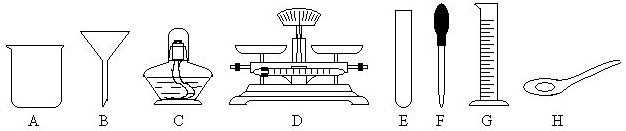
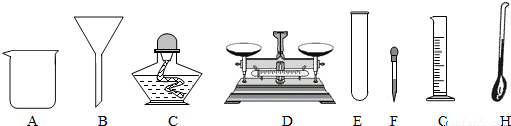
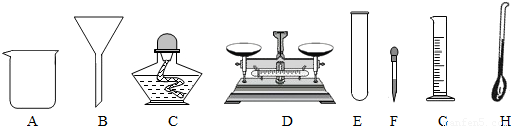
(3)进行蒸发时除了用到铁架台、铁圈和下述提供的仪器外还缺的仪器是
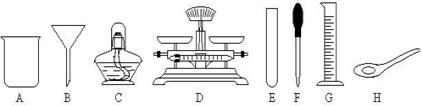
(4)过滤时,某同学向漏斗倾倒液体,不小心使漏斗的液面超过了滤纸的边缘,这时,该同学应进行的操作是
(1)通过长颈漏斗向放有块状碳酸钙的大试管中加入足量的盐酸,充分反应,在大试管中可以观察到的现象是
有大量气泡产生,块状固体逐渐消失
(2)反应完毕,欲从反应液中制取少量纯净的氯化钙晶体,拟进行下列几项操作:
①蒸发 ②过滤 ③加入适量的X溶液
X的化学式是
Ca(OH)2
;上述几项操作正确的顺序是③②①
(填序号)(3)进行蒸发时除了用到铁架台、铁圈和下述提供的仪器外还缺的仪器是
蒸发皿
、玻璃棒
,其中玻璃棒
(填仪器名称)是进行过滤和蒸发时都要使用,但使用目的各不相同的玻璃仪器.
(4)过滤时,某同学向漏斗倾倒液体,不小心使漏斗的液面超过了滤纸的边缘,这时,该同学应进行的操作是
制作新的过滤器,重新过滤
.分析:(1)通过块状物体与盐酸的化学反应的生成物来作答;
(2)在(1)中,可能有剩余的盐酸,在加入X物质时,应考虑该物质X能与盐酸发生化学反应,并能产生氯化钙,只有这样才能从反应液中制取少量纯净的氯化钙晶体;
(3)在蒸发这一环节中,必须使用蒸发皿和玻璃杯;
(4)在过滤中,从过滤纸的作用方面来解释.
(2)在(1)中,可能有剩余的盐酸,在加入X物质时,应考虑该物质X能与盐酸发生化学反应,并能产生氯化钙,只有这样才能从反应液中制取少量纯净的氯化钙晶体;
(3)在蒸发这一环节中,必须使用蒸发皿和玻璃杯;
(4)在过滤中,从过滤纸的作用方面来解释.
解答:解:(1)通过长颈漏斗向放有块状碳酸钙的大试管中加入足量的盐酸,充分反应,其反应过程为:
碳酸钙+盐酸→氯化钙+水+二氧化碳↑
碳酸镁+盐酸→氯化镁+水+二氧化碳↑
该反应中的块状固体碳酸钙、碳酸镁在与足量的盐酸反应后,逐渐消失了,另外,在反应过程中,不断有二氧化碳气体冒出.所以,在大试管中可以观察到的现象是:有大量气泡产生,块状固体逐渐消失;
(2)在(1)中,因为加入了足量的盐酸,所以,在块状物体与盐酸的反应充分后,会有盐酸剩余.既要出去多余的盐酸,又要使氯化钙晶体中没有杂质,加入的适量的X溶液最好既能与盐酸发生反应,又不产生异于氯化钙的物质;
(3)进行蒸发时除了用到铁架台、铁圈和下述提供的仪器外还缺的仪器是蒸发皿,因为用于溶液蒸发或浓缩的仪器是蒸发皿;另外,在蒸发过程中,需要有玻璃杯搅拌液体,在过滤过程中,玻璃杯起引流的作用;
(4)过滤时,滤纸的作用是过滤液体中的杂质,如果液面高于滤纸会使一部分液体在漏斗与滤纸的夹缝中流走导致过滤不彻底,这样滤纸就徒劳无功了.
所以,本题的答案为:
(1)有大量气泡产生,块状固体逐渐消失;
(2)Ca(OH)2、③②①;
(3)蒸发皿、玻璃棒,玻璃棒;
(4)制作新的过滤器,重新过滤.
碳酸钙+盐酸→氯化钙+水+二氧化碳↑
碳酸镁+盐酸→氯化镁+水+二氧化碳↑
该反应中的块状固体碳酸钙、碳酸镁在与足量的盐酸反应后,逐渐消失了,另外,在反应过程中,不断有二氧化碳气体冒出.所以,在大试管中可以观察到的现象是:有大量气泡产生,块状固体逐渐消失;
(2)在(1)中,因为加入了足量的盐酸,所以,在块状物体与盐酸的反应充分后,会有盐酸剩余.既要出去多余的盐酸,又要使氯化钙晶体中没有杂质,加入的适量的X溶液最好既能与盐酸发生反应,又不产生异于氯化钙的物质;
(3)进行蒸发时除了用到铁架台、铁圈和下述提供的仪器外还缺的仪器是蒸发皿,因为用于溶液蒸发或浓缩的仪器是蒸发皿;另外,在蒸发过程中,需要有玻璃杯搅拌液体,在过滤过程中,玻璃杯起引流的作用;
(4)过滤时,滤纸的作用是过滤液体中的杂质,如果液面高于滤纸会使一部分液体在漏斗与滤纸的夹缝中流走导致过滤不彻底,这样滤纸就徒劳无功了.
所以,本题的答案为:
(1)有大量气泡产生,块状固体逐渐消失;
(2)Ca(OH)2、③②①;
(3)蒸发皿、玻璃棒,玻璃棒;
(4)制作新的过滤器,重新过滤.
点评:本题综合考查了混合物的分离方法、实验步骤的研究、过滤的原理、方法及其注意事项(过滤液体时,要注意一贴二低三靠的原则.即一贴:用少量水润湿的滤纸要紧贴漏斗壁,二低:滤纸边缘低于漏斗边缘、滤液低于滤纸边缘,三靠:烧杯紧靠玻璃棒、玻璃棒靠在三层滤纸上、漏斗下端口紧靠烧杯内壁).

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目