题目内容
在氧化铜和铁粉的混合物中,加入一定量的稀硫酸,微热,待反应停止后过滤,再向滤液中放一枚铁钉,过一会儿取出,发现铁钉无变化,根据上述现象作出的判断中正确的是
- A.不溶物一定是铜
- B.不溶物一定是铁
- C.滤液是硫酸亚铁溶液
- D.滤液是硫酸亚铁和硫酸铜的混合溶液
C
分析:根据铁及CuO等物质的有关化学性质.分析时若仅仅看到CuO与H2SO4以及Fe与H2SO4的反应就易错解.如果能抓住“未看到铁片有任何变化”这个条件,并结合铁的化学性质,便能正确作答.
解答:根据金属活动顺序可知向滤液中加入薄铁片,铁片无任何变化,说明加入的稀硫酸少量或恰好完全反应,同时也说明滤液中没有硫酸铜和硫酸.
A、滤液中没有硫酸和硫酸铜,说明不溶物中一定有铜,但铁是否反应完无法确定,故也可能有铁,故A错误;
B、滤液中没有硫酸和硫酸铜,说明不溶物中有铜,但铁是否反应完无法确定,所以铁可能含有也可能不含有,故B错误;
C、因为硫酸和铁参加了反应,所以滤液中一定有硫酸亚铁,但由于滤液和铁不反应,所以滤液中没有硫酸和硫酸铜,故C正确;
D、再向滤液中放一枚铁钉,过一会儿取出,发现铁钉无变化,说明滤液中没有硫酸和硫酸铜,故D错误.
故选:C.
点评:此题是一道推断知识考查题,解题的关键是对最后加入铁后无变化的分析,也就是说明反应后的溶液中不会有硫酸铜及硫酸的存在,这是解题的关键.
分析:根据铁及CuO等物质的有关化学性质.分析时若仅仅看到CuO与H2SO4以及Fe与H2SO4的反应就易错解.如果能抓住“未看到铁片有任何变化”这个条件,并结合铁的化学性质,便能正确作答.
解答:根据金属活动顺序可知向滤液中加入薄铁片,铁片无任何变化,说明加入的稀硫酸少量或恰好完全反应,同时也说明滤液中没有硫酸铜和硫酸.
A、滤液中没有硫酸和硫酸铜,说明不溶物中一定有铜,但铁是否反应完无法确定,故也可能有铁,故A错误;
B、滤液中没有硫酸和硫酸铜,说明不溶物中有铜,但铁是否反应完无法确定,所以铁可能含有也可能不含有,故B错误;
C、因为硫酸和铁参加了反应,所以滤液中一定有硫酸亚铁,但由于滤液和铁不反应,所以滤液中没有硫酸和硫酸铜,故C正确;
D、再向滤液中放一枚铁钉,过一会儿取出,发现铁钉无变化,说明滤液中没有硫酸和硫酸铜,故D错误.
故选:C.
点评:此题是一道推断知识考查题,解题的关键是对最后加入铁后无变化的分析,也就是说明反应后的溶液中不会有硫酸铜及硫酸的存在,这是解题的关键.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案
相关题目
在氧化铜和铁粉的混合物中,加入一定量的稀硫酸,微热,待反应停止后过滤,再向滤液中放一枚铁钉,过一会儿取出,发现铁钉无变化,根据上述现象作出的判断中正确的是( )
| A、不溶物一定是铜 | B、不溶物一定是铁 | C、滤液是硫酸亚铁溶液 | D、滤液是硫酸亚铁和硫酸铜的混合溶液 |

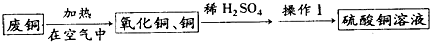
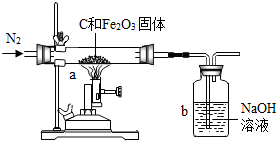 (2012?鼓楼区一模)化学兴趣小组的同学为了测定某赤铁矿石中氧化铁的质量分数.
(2012?鼓楼区一模)化学兴趣小组的同学为了测定某赤铁矿石中氧化铁的质量分数.