题目内容
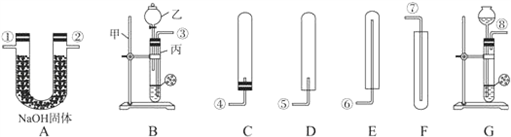
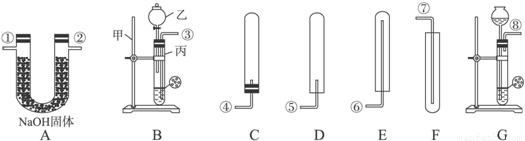
(6分)下图所示为实验室中常见的气体制备、净化、收集和性质实验的部分仪器。试根据题目要求,回答下列问题:

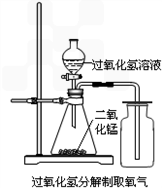
(1)若以过氧化氢溶液为原料(二氧化锰作催化剂)在实验室中制备并收集干燥的氧气。
①所选仪器的连接顺序为A → → 。
②仪器A中发生的化学方程式是 。
(2)若用含少量CO2的CO气体测定某不纯Fe2O3样品的纯度(杂质不含铁),仪器的连接顺序为,混合气体→C1→B→D→C2(C1、 C2为两个盛有澄清石灰水的仪器)
①C2中的现象为 ,化学方程式为 。
②通过测定C2质量的变化来计算Fe2O3样品的纯度,若不连接C1,则计算出的结果
将 (填“偏大”“偏小”“不受影响”)。
③从环保的角度分析,此装置设计的不足之处 。
(6分)B F ; 2H2O2====2H2O+O2↑;变浑浊 ; Ca(OH)2+CO2==CaCO3↓+H2O
偏大; 无尾气处理装置,污染环境。
解析:氧气密度比空气大,所以要选择F装置来收集氧气,要求收集干燥的氧气的氧气,所以需要用到B装置使用浓硫酸来干燥一下,故(1)①填B F.过氧化氢分解方程式为2H2O2====2H2O+O2↑,二氧化碳可以使澄清石灰水变浑浊,反应方程式为Ca(OH)2+CO2==CaCO3↓+H2O。若不连接C1,C2的质量会偏大,所以结果会偏大。此装置设计的不足之处是一氧化碳有毒,无尾气处理装置,会污染环境。

练习册系列答案
相关题目