题目内容
(09宿迁)2009年6月1日,国家《食品安全法》正式实施,在食品行业中“免
检”一词已成为历史,“凡食品必检、不合格不上市”成为最基本原则。某检测站对某品牌
奶粉进行检测。取该奶粉样品100g,使其中蛋白质中的氮元素完全转变成氨气,用50g溶
质质量分数为9.8%的稀硫酸恰好完全吸收【2NH3+H2SO4=(NH4)2SO4】。计算并回答下列问题:
(1)产生氨气的质量。
(2)该奶粉中含氮元素的质量分数。
(3)奶粉中蛋白质含量的国家标准为:每100g奶粉中含蛋白质12g—25g。 蛋白质中氮元
素的平均质量分数为16%,则合格奶粉中氮元素的质量分数范围为 ;通过对比说明
上述检测的奶粉是否合格?
(4)上述奶粉若不合格,不法奶商为使其“合格”,常在奶粉中添加化工原料三聚氰胺(化学式C3N6H6),以提升奶粉检测中的含氮量,造成蛋白质达标的假象。请你计算100g上述不合格奶粉中至少需要加入多少克三聚氰胺,才能成为“合格”奶粉。
(友情提醒:2/3-0.0192≈0.65
检”一词已成为历史,“凡食品必检、不合格不上市”成为最基本原则。某检测站对某品牌
奶粉进行检测。取该奶粉样品100g,使其中蛋白质中的氮元素完全转变成氨气,用50g溶
质质量分数为9.8%的稀硫酸恰好完全吸收【2NH3+H2SO4=(NH4)2SO4】。计算并回答下列问题:
(1)产生氨气的质量。
(2)该奶粉中含氮元素的质量分数。
(3)奶粉中蛋白质含量的国家标准为:每100g奶粉中含蛋白质12g—25g。 蛋白质中氮元
素的平均质量分数为16%,则合格奶粉中氮元素的质量分数范围为 ;通过对比说明
上述检测的奶粉是否合格?
(4)上述奶粉若不合格,不法奶商为使其“合格”,常在奶粉中添加化工原料三聚氰胺(化学式C3N6H6),以提升奶粉检测中的含氮量,造成蛋白质达标的假象。请你计算100g上述不合格奶粉中至少需要加入多少克三聚氰胺,才能成为“合格”奶粉。
(友情提醒:2/3-0.0192≈0.65
(1)设产生氨气的质量为x
2NH3+H2SO4="=" (NH4)2SO4
34 98
x 50g×9.8% 34/ x = 98/50g×9.8% (1分)
x =1.7g 氨气的质量为1.7g (1分)
(2)N% =( 1.7g ×14/17)/100g×100% = 1.4% (2分)
(3)1.92%~4% (1分) ∵1.4%﹤1.92% ∴奶粉不合格 (1分)
(4)设至少需要加入yg三聚氰胺
100g×1.4% ﹢y×84/126 = (100g﹢y) ×1.92% (2分)
 y = 0.8g 至少需要加入0.8g三聚氰胺 (1分)
y = 0.8g 至少需要加入0.8g三聚氰胺 (1分)
2NH3+H2SO4="=" (NH4)2SO4
34 98
x 50g×9.8% 34/ x = 98/50g×9.8% (1分)
x =1.7g 氨气的质量为1.7g (1分)
(2)N% =( 1.7g ×14/17)/100g×100% = 1.4% (2分)
(3)1.92%~4% (1分) ∵1.4%﹤1.92% ∴奶粉不合格 (1分)
(4)设至少需要加入yg三聚氰胺
100g×1.4% ﹢y×84/126 = (100g﹢y) ×1.92% (2分)
 y = 0.8g 至少需要加入0.8g三聚氰胺 (1分)
y = 0.8g 至少需要加入0.8g三聚氰胺 (1分)分析:(1)根据氨气与硫酸反应的化学方程式,由吸收氨气消耗硫酸的质量计算氨气的质量;
(2)根据检测蛋白质的方法可知,所吸收氨气中的N元素质量即所取100g奶粉样品中N元素的质量,利用奶粉中含氮元素的质量分数=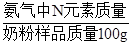 ×100%可完成计算;
×100%可完成计算;
(3)根据蛋白质中氮元素的平均质量分数为16%,
利用奶粉中氮元素的质量分数= ×100%,计算100g奶粉中含蛋白质12g~25g时氮元素的质量分数范围;利用所取奶粉样品中N元素的质量分数与国家标准对比,判断所取奶粉是否合格;
×100%,计算100g奶粉中含蛋白质12g~25g时氮元素的质量分数范围;利用所取奶粉样品中N元素的质量分数与国家标准对比,判断所取奶粉是否合格;
(4)奶粉中添加三聚氰胺后其中N元素一部分来自奶粉中蛋白质另一部分来自添加的三聚氰胺,计算使得添加后的奶粉中N元素质量分数达到国家最低标准时所添加量.
解:(1)设产生氨气的质量为x
2NH3+H2SO4═(NH4)2SO4
34 98
x 50g×9.8%
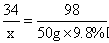
x=1.7g
(2)该奶粉中含氮元素的质量分数=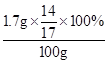 ×100%=1.4%
×100%=1.4%
(3)每100g奶粉中含蛋白质12g,奶粉中氮元素的质量分数=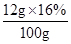 ×100%=1.92%
×100%=1.92%
每100g奶粉中含蛋白质25g,奶粉中氮元素的质量分数=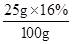 ×100%=4%
×100%=4%
则合格奶粉中氮元素的质量分数范围为1.92%~4%,
∵1.4%<1.92%
∴奶粉不合格
(4)设至少需要加入三聚氰胺质量为y
100g×1.4%﹢y×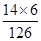 ×100%=(100g﹢y)×1.92%
×100%=(100g﹢y)×1.92%
y=0.8g
答:(1)氨气的质量为1.7g;
(2)该奶粉中含氮元素的质量分数为1.4%;
(3)奶粉不合格;
(4)至少需要加入0.8g三聚氰胺.
(2)根据检测蛋白质的方法可知,所吸收氨气中的N元素质量即所取100g奶粉样品中N元素的质量,利用奶粉中含氮元素的质量分数=
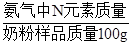 ×100%可完成计算;
×100%可完成计算;(3)根据蛋白质中氮元素的平均质量分数为16%,
利用奶粉中氮元素的质量分数=
 ×100%,计算100g奶粉中含蛋白质12g~25g时氮元素的质量分数范围;利用所取奶粉样品中N元素的质量分数与国家标准对比,判断所取奶粉是否合格;
×100%,计算100g奶粉中含蛋白质12g~25g时氮元素的质量分数范围;利用所取奶粉样品中N元素的质量分数与国家标准对比,判断所取奶粉是否合格;(4)奶粉中添加三聚氰胺后其中N元素一部分来自奶粉中蛋白质另一部分来自添加的三聚氰胺,计算使得添加后的奶粉中N元素质量分数达到国家最低标准时所添加量.
解:(1)设产生氨气的质量为x
2NH3+H2SO4═(NH4)2SO4
34 98
x 50g×9.8%
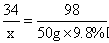
x=1.7g
(2)该奶粉中含氮元素的质量分数=
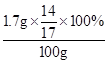 ×100%=1.4%
×100%=1.4%(3)每100g奶粉中含蛋白质12g,奶粉中氮元素的质量分数=
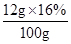 ×100%=1.92%
×100%=1.92%每100g奶粉中含蛋白质25g,奶粉中氮元素的质量分数=
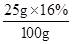 ×100%=4%
×100%=4%则合格奶粉中氮元素的质量分数范围为1.92%~4%,
∵1.4%<1.92%
∴奶粉不合格
(4)设至少需要加入三聚氰胺质量为y
100g×1.4%﹢y×
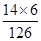 ×100%=(100g﹢y)×1.92%
×100%=(100g﹢y)×1.92% y=0.8g
答:(1)氨气的质量为1.7g;
(2)该奶粉中含氮元素的质量分数为1.4%;
(3)奶粉不合格;
(4)至少需要加入0.8g三聚氰胺.

练习册系列答案
 全程金卷系列答案
全程金卷系列答案
相关题目