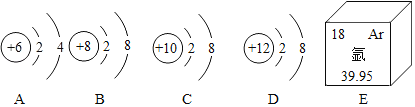题目内容
【题目】根据下列粒子结构示意图,回答问题。
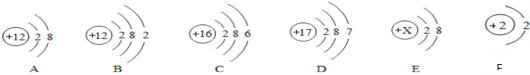
(1)上图A、B、C、D四种粒子共表示_____种元素;
(2)D原子在化学反应中易_____(填“得到”或“失去”)电子;
(3)上图从A至F中达到相对稳定结构的是_____;
(4)E粒子带1个单位负电荷,则X=_____。
【答案】三 得到 A、E、F 9
【解析】
(1)元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),A、B、C、D四种粒子的核内质子数分别是12、12、16、17,共表示3种元素;
(2)D原子的最外层电子数是7,在化学反应中易得到1个电子而形成阴离子;
(3)最外层电子数是8(氦是2)属于稳定结构,故上图从A至F中达到相对稳定结构的是:A、E、F;
(4)E粒子带1个单位正电荷,是原子得到1个电子形成的,则X=2+8-1=9。

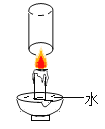
【题目】为探究碳还原氧化铜的最佳实验条件用木炭粉和氧化铜的干燥混合物1~2.5g,甪如图所示装置进行实验。

(1)碳还原氧化铜的化学方程式为__________,证明生成了二氧化碳的现象是__________。
(查阅资料)①氧化铜(![]() )为黑色固体。
)为黑色固体。
②碳还原氧化铜得到的铜中可能含有少量的氧化亚铜;氧化亚铜为红色固体,能与稀硫酸反应:![]() 。
。
(进行实验)取一定量的混合物,用上图装置进行实验。
序号 | 木炭粉与氧化铜的质量比 | 反应后物质的颜色、状态 | |
1 | 1:9 | 红色固体有金属光泽 | 混有少量黑色物质 |
2 | 1:10 | 混有很少量黑色物质 | |
3 | 1:11 | 混有极少量黑色物质 | |
4 | 1:12 | 无黑色物质 | |
5 | 1:13 | 混有较多黑色物质 | |
(解释与结论)(2)由此得到的结论是__________。
(反思与评价)(3)实验2没有进行质量比为1:14的实验,理由是__________。
(4)为检验生成的红色固体中是否含![]() ,所需试剂是__________。
,所需试剂是__________。