题目内容
【题目】(5分)用如图实验方法分离NaCl和CaCl2两种固体的混合物A,根据操作流程完成下列问题: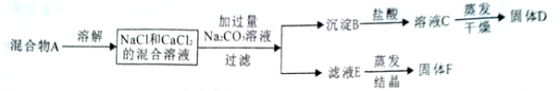
(1)B物质是 .
(2)过滤操作中玻璃棒的作用是 .
(3)经分析上述方法分离出的F含杂质,请对该设计方案加以完善 .
(4)若用原操作方法,要测出混合物A中NaCl和CaCl2的质量比,不称量D,可通过称量 和 的质量求解.
【答案】(1)碳酸钙(或CaCO3) (2)引流
(3)蒸发前先加适量的盐酸至不再产生气泡 (4)A B
【解析】
试题分析:(1)CaCl2溶液会与加入的Na2CO3溶液发生反应:CaCl2+Na2CO3==CaCO3↓+2NaCl,故沉淀B物质是碳酸钙(或CaCO3)
(2)过滤操作中玻璃棒的作用是引流
(3)由于所加的Na2CO3溶液是过量的,故经过过滤后所得的滤液E中除了NaCl,还有过量的Na2CO3,所以为了得到纯净的NaCl,还应将杂质Na2CO3除去,可设计方案:蒸发前先加适量的盐酸至不再产生气泡
(4)若用原操作方法,要测出混合物A中NaCl和CaCl2的质量比,不称量D,可通过称量A 和B的质量来求解

【题目】育才中学的某研究小组在探究维生素C水溶液的酸碱性时,不慎误把维C泡腾片(保健品。主要成分如图所示)当做维生素C片放入了水中,结果发现有大量气泡产生,于是引起了该小组同学的探究性趣。

【提出问题】该气体成分是什么?
【猜想与假设】小青说:该气体可能含有CO2、O2、CO、H2、N2中的一种或几种。小丽说:不可能含有N2,因为
小亮说:不可能含有H2 和CO,因为从药品安全角度考虑,H2易燃易爆,CO 最后研究小组的同学共同认为:该气体可能含有CO2 、O2中的一种或两种。
编号 | 实验操作 | 实验现象 |
① | 将气体通入澄清的石灰水 | 澄清石灰水变浑浊 |
② | 将带火星的木条伸入到该气体中 | 带火星的木条没有复燃 |
【进行实验】
编号 | 实验操作 | 实验现象 |
① | 将气体通入澄清的石灰水 | 澄清石灰水变浑浊 |
② | 将带火星的木条伸入到该气体中 | 带火星的木条没有复燃 |
【得出结论】(1)由实验①可知,该气体中肯定含有 ,写出该反应的化学方程式 ;(2)由实验② (填“能”或“不能”)确定该气体中不含氧气,理由是 。