题目内容
【题目】为进一步认识氧气,老师邀请你一起参加《性质活泼的氧气》的研究。请根据下图所示装置回答问题:
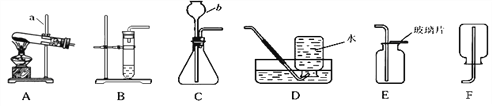
(1) 某同学选用A装置制取氧气,在连接玻璃管和带孔橡皮塞时,玻璃管不容易插入橡皮塞,应采取的措施是:_____。在试管中装入暗紫色的固体物质,则反应的化学方程式为 __________;该反应属于_________反应。
(2)实践证明用B装置制氧气比A装置具有很多优点,主要优点有________(填字母序号)。
A.安全 B.气密性好 C.节约能源 D.产生氧气多
(3)某同学选用C装置制取氧气,长颈漏斗的下端没有伸到液面以下,其后果是________。
(4)若用D装置收集氧气,发现氧气不纯,可能原因是______________。(答一点)
(5)通过查阅资料得知:氨气(NH3)是一种密度比空气小且极易溶于水的气体,其水溶液称为氨水;实验室用加热氯化铵和氢氧化钙的固体混合物制取氨气。
根据以上信息,实验室制取氨气时,应选择上图中的________装置。(填字母编号)
(6)实验结束,同学们就检查装置的气密性展开讨论,大家提出除了用手紧握的方法外,还可以用什么方法?甲同学的方案得到一致认同:以装置B为例,在导气管上外接一段橡皮管和长约20cm—30 cm的直玻璃管,将玻璃管一端浸入烧杯内的水中(如下图,部分装置省略),保持装置的温度不变,水进入玻璃管一段高度后,不再进入。若装置气密性良好,则进入玻璃管的液面________ 烧杯中液面。(填字母符号)
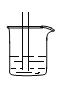
A.高于 B.低于 C. 相平 D. 无法判断
【答案】 将导管口用水湿润 略 分解反应 A C 产生的氧气从长颈漏斗中逸出 导管口一有气泡就收集(或集气瓶没有装满水) A F B
【解析】(1)在连接玻璃管和带孔橡皮塞时,玻璃管不容易插入橡皮塞,应采取的措施是:将橡胶塞湿润,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,反应的化学方程式为 :2KMnO4△ K2MnO4+MnO2+O2↑,该反应属于分解反应;(2)通过分析装置A、B的反应条件、生成物可知,用B装置制氧气比A装置具有的主要优点有:节约能源,故选:C;(3)选用C装置制取氧气,仪器b的下端没有伸到液面以下,后果是:氧气从长颈漏斗逸出;(4)用排水法收集氧气,发现氧气不纯,可能原因是:导管口一有气泡就收集(或集气瓶没有装满水) ;(5)实验室制取氨气的反应物是固体,反应条件是加热,氨气密度比空气小且极易溶于水,所以实验室制取氨气时,应选择上图中的AF装置;(6)检验装置的气密性的方法是:先把导管的一端放入水中,然后两手紧握试管的外壁,观察导管口是否有气泡冒出,故选:B。

 阅读快车系列答案
阅读快车系列答案【题目】实验探究一:课本第二单元课后作业中有“寻找新的催化剂” 的探究内容,实验中学探究小组据此设计了如下探究方案。
【提出问题】红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
【实验探究】
实验步骤 | 实验现象 | 实验结论及解释 |
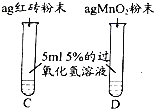
Ⅰ. | A中无明显现象, B中产生大量能使带火星木条复燃的气体 | ① 产生的气体是______ ② 红砖粉末能改变过氧化氢分解速率 |
Ⅱ. 向B试管中重新加入5%的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣 | ① 又产生大量能使带火星木条复燃的气体 ② 滤渣质量等于ag | 红砖粉末的_____在反应前后均没有发生变化,能作过氧化氢分解的催化剂 |
Ⅲ. | 两试管中均产生气泡且______ | 红砖粉末的催化效果没有二氧化锰粉末好 |
【拓展应用】己知CuSO4也可作为过氧化氢分解的催化剂。写出其反应的符号表达式___________________________