题目内容
【题目】一包固体,可能含有锌粉、碳粉、氧化铜、氢氧化钾、氯化钠中的一种或几种。为探究固体组成,某化学兴趣小组进行了如下图所示的实验。
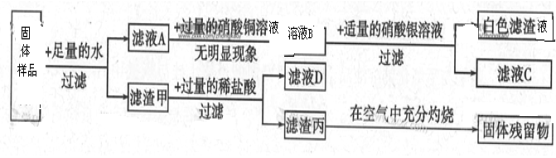
请回答下列问题:
(1)该实验中生成白色滤渣乙的化学方程式为 。
(2)原固体中一定不含有的物质是 。
(3)原固体中一定含有的物质是 。
【答案】 (1)NaCl+AgNO3=AgCl↓+NaNO3
(2)KOH (3)Zn、CuO、NaCl
【解析】氧化铜、锌粉、碳粉都不溶于水,碳粉不溶于酸,氢氧化钾和硝酸铜会生成氢氧化铜沉淀,氯化钠和硝酸银会生成氯化银沉淀,所以(1)生成白色沉淀滤渣乙的反应是氯化钠和硝酸银反应生成氯化银沉淀和硝酸钠,化学方程式为:NaCl+AgNO3=AgCl↓+NaNO3;(2)通过推导可知,原固体中一定不含有的物质是氢氧化钾,原因是:滤液A中加入过量的硝酸铜溶液,无明显现象;(3)加入一定量的硝酸银溶液会生成白色沉淀,所以混合物中一定含有氯化钠;加入过量的稀盐酸,生成的滤渣丙在空气中灼烧,有固体残留;所以原固体中一定含有的物质是氯化钠、氧化铜、锌;

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目