题目内容
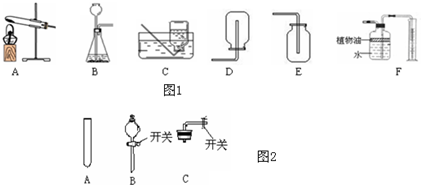
 根据如图的装置图回答问题:
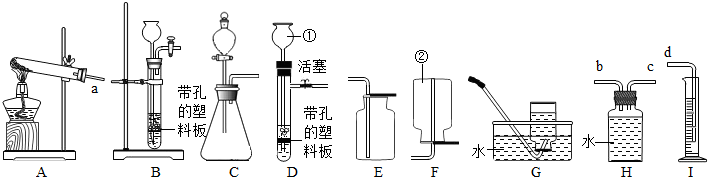
根据如图的装置图回答问题:(1)装置D中除导管外的两种仪器的名称分别是
水槽
水槽
、集气瓶
集气瓶
.(2)用高锰酸钾制取并收集氧气时可选择的装置为
BD
BD
(填序号,下同).如改用过氧化氢溶液和二氧化锰制取氧气时,应选择的发生装置为A
A
.(3)比较上述两种制取氧气的方法,你认为选择
过氧化氢
过氧化氢
(填过氧化氢或高锰酸钾)更好一些,理由是在常温下反应,可以控制氧气流速
在常温下反应,可以控制氧气流速
.分析:水槽是盛水的仪器,集气瓶是收集气体的仪器;制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.用过氧化氢制取的方法更好一些,因为在常温下反应,可以控制氧气流速,节约能源等.
解答:解:(1)水槽是盛水的仪器,集气瓶是收集气体的仪器,故答案为:水槽;集气瓶;
(2)如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;故答案为:BD;A;
(3)用过氧化氢制取的方法更好一些,因为在常温下反应,可以控制氧气流速,节约能源等;故答案为:过氧化氢;在常温下反应,可以控制氧气流速.
(2)如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;故答案为:BD;A;
(3)用过氧化氢制取的方法更好一些,因为在常温下反应,可以控制氧气流速,节约能源等;故答案为:过氧化氢;在常温下反应,可以控制氧气流速.
点评:本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目